Comprendre la loi des gaz parfaits par la mécanique des molécules
PDF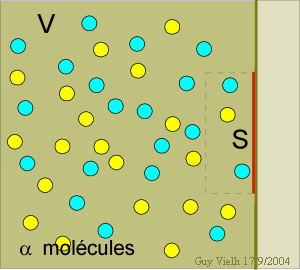
En multipliant par la quantité de mouvement 2 m u apportée par chaque molécule et en divisant par la surface, on obtient ainsi la pression p = (N/V) mu2.
La vitesse u de chaque molécule dépend du hasard des chocs qu’elle subit. La pression résulte de la moyenne de u2 sur toutes les molécules, notée <u2>. La formule précédente donne donc pV = Nm<u2>. La comparaison avec la loi des gaz parfaits permet ainsi de relier l’énergie cinétique des molécules (1/2)m<u2> à la température par (1/2)m<u2> = (1/2)kBT.
Les molécules se déplacent en fait avec un vecteur vitesse u dans toutes les directions, et selon le théorème de Pythagore, u2 = u2+v2+w2, ou u, v, w sont les projections des vitesses selon chaque coordonnée. Celles-ci sont identiques en moyenne dans toutes les directions, <u2>=<u2>+<v2>+<w2>=3<u2>, ce qui permet d’exprimer l’énergie cinétique totale de translation des molécules comme (1/2)m<u2> = (3/2)kBT.
Les chocs sur la paroi ne sont pas élastiques comme nous l’avons supposé ici : les molécules échangent de l’énergie avec les atomes de la paroi. Cependant à l’équilibre thermique, il n’y a pas d’échange net d’énergie entre le gaz et la paroi, ce qui valide l’hypothèse d’un choc élastique en moyenne. De même les molécules n’échangent pas en moyenne de quantité de mouvement tangentiellement à la paroi, car leur vitesse le long de la paroi est nulle en moyenne. Il n’y a donc pas de force tangentielle. Il n’en serait plus de même en présence d’un écoulement le long de la paroi qui s’accompagne d’une force tangentielle de viscosité.




