玻璃:持久性的材料

玻璃无处不在,已经成为我们生活中必不可少的材料。 它具有透明、坚硬、耐用、可着色、可无限循环利用等卓越特性,不会造成太大的污染。众所周知,玻璃是由沙子的主要成分二氧化硅制成的,玻璃制造技术和工艺由来已久,各种功能独特的玻璃纷纷问世,并且日新月异。每种玻璃的特性和用途均取决于其化学成分、分子结构和制造技术。本文内容节选自即将出版的新书《玻璃,持久性的材料》[1]。
1. 玻璃,无处不在的材料
全球每年玻璃的产量约为1.8亿吨(其中欧洲超过 4,000 万吨),玻璃行业分布在世界各地,并且产量极大,下表详细列出了欧洲各工业门类的玻璃产量。
目前玻璃市场规模约为2000亿美元,且每年持续增长率接近5%。玻璃的制造工艺相对简单,自古以来就可以回收利用。如今在欧洲,玻璃回收是将碎玻璃添加到沙子和碳酸钠等原材料中煅烧来进行的。玻璃制造之所以能够长久地存在并在生活中随处可见,是因为它具有着叹为观止的独特性能。
1.1 透明性
玻璃具有非凡特性,几个世纪以来一直是人们日常生活中不可或缺的一部分。几千年来,其透明性这种卓越特点俘获了人们的心意。在二十世纪下半叶塑料出现之前,玻璃是唯一一种价格亲民又可大量生产的透明材料。除了罕见的单晶外,玻璃的透明特性无与伦比。

光线不受阻碍即可穿过玻璃的能力,即玻璃的透光性使得它被广泛应用于各个领域,特别是光学领域。玻璃是我们探索世界能力的奥秘,通过玻璃,我们可以直观地观察到小到细胞的微观结构,大到遥远的宇宙空间。显微镜的玻璃透镜揭示了微观的细节,而望远镜和天文透镜则反映出天体的奇观。
这种玻璃的透明属性也变成了日常生活的一部分,窗户将我们与外部世界联系起来,为建筑物提供了自然光和真实的美感。艺术家们通过为玻璃着色创造出精美的作品,这一传统可以追溯到数千年以前。
1.2 耐用、坚固

玻璃不仅透明,而且经久耐用,凡尔赛宫镜厅里有着数百年历史的镜子和沙特尔大教堂有着数千年历史的彩绘玻璃窗(图1)就可以证明这一点,它们不但可以透光,而且外边也无从了解里边。玻璃是一种化学中性材料,它不会与其它物质发生化学反应,无论是气体、液体还是固体,因此成为炼金士和化学家的理想工具,随着时间的推移,玻璃材料和工艺得到了改进和加强,它们可以承受更高的温度,这对于配有微晶玻璃灶具的现代厨房至关重要(见图9)。玻璃的机械强度决定了其抗拉强度和抗压强度,玻璃之所以得到广泛应用,原因之一就是其抗压和抗拉强度高。就硬度而言,玻璃也是一种特别的材料,不易被刮花,除非采用像钻石一样硬度更高且稀有的材料去划它。在巴黎拉佩鲁兹(Lapérouse)餐厅的镜子上依然留有钻石的划痕(图2)。
玻璃还可用于溶解矿物质,特别是可以在核废料处理中用作基质。作为一种电绝缘体,它在电诞生之初就具有重要价值,其电学特性在现代应用中仍继续发挥着至关重要的作用。
1.3 粘度
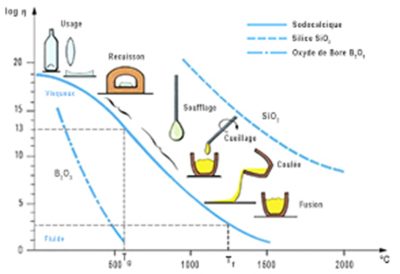
玻璃另一个有巨大吸引力的特性就是它的粘度会随温度变化而变化(图3)。无论是历史悠久、至今仍被沿用的吹制工艺(图4),还是制造平板玻璃的现代工艺(浮法工艺 [2]),利用这一特性可以实现独特的造型,通过各种工艺“塑造”玻璃。
1.4 可回收性

玻璃如今在世界许多国家的回收产业中都扮演着关键角色。玻璃的大部分卓越性能源于其微观上原子排列无定形的非晶特性[3],21世纪物理学家仍然在讨论这个话题。玻璃这种持久的材料,继续以无法估量的方式启示和服务于人类。这种在微观上呈现无序的材料区别于原子有序排列二氧化硅晶体,它的微观原子是随机排列的。这种无序的晶体结构正是其独特性质的根源所在,它所具有的透明性,还有随温度变化而变化的粘度,造就了它的独特成型特性。
2. 玻璃的起源
2.1 泡碱:提取玻璃的矿石
玻璃的发现和历史可以追溯到古代文明时期,充满着神秘和传奇色彩。老普林尼在其著作《自然史》[4]中讲述了一个浪漫的故事:腓尼基商人在寻找石头来架锅时发现了玻璃。他们用泡碱石(natron)(一种含有碳酸钠的石头)来架锅(图5)。在火的炙烤下,泡碱石与贝卢斯河岸的沙子熔合在一起,产生了一种未知的材料,流淌成透明的小溪,相传这就是玻璃的由来[5]。

https://www.mediachimie.org/sites/default/files/NAT-GO23-D4-verre.pdf, DR]
产生这种现象的原因是钠与沙子中的二氧化硅(SiO2)在高温下发生了反应。钠降低了二氧化硅的熔点,但这并不是简单的熔合。物质并非突然从固态变为液态,而是在约800°C时逐渐变软,在大约1000°C 左右时变成类似蜂蜜的 “液体”,温度越高,粘度越低。因此,钠和二氧化硅在高温下结合产生了玻璃。虽然这一解释在历史学家中引起过一些争议,但仍然是关于玻璃诞生的动人故事。
无论这个故事的真实性如何,现在我们都知道早在公元前一千多年前就开始制造玻璃。当时,许多玻璃生产中心为地中海地区提供 “生玻璃”,也称为粗制玻璃。然后,在离消费者最近的地方对粗制玻璃进行加工。
2.2 钠以外的助熔剂
玻璃制造中的关键是添加助熔剂, 比如钠(俗称 “苏打”),有助于降低二氧化硅的熔点,同时促使玻璃粘度的持续变化。人们很快就发现钠硅玻璃耐水性较差,随着时间的推移,容易老化。添加钙,主要是碳酸钙(俗称 “石灰”),可以延缓老化速度。硅、钠和钙(图3中用实线表示)是制备钠钙玻璃的基本元素,这也是现代玻璃最常见的配方之一,尽管还有一些其他成分。
钠并非唯一可用的助熔剂,钾和硼也具有这种作用。除了钠,从古代文明时期,钾也被广泛使用,它主要来自植物燃烧的灰烬。在难以找到泡碱的地区,可以选用其他助熔剂对玻璃工业而言也是一大优势。玻璃材料能从固态凝固到液态,中间还会呈现粘稠的玻璃态。玻璃工匠们开发利用以上特性,采用吹制工艺制造玻璃器具(见图 4),在一些古书中均有图谱记载。玻璃的这种独特的成型能力在其历史和应用中发挥了关键作用。
3. 为什么玻璃具有这些特性?
3.1 玻璃为什么透明?
透明性是固体材料的一种特殊性质,直到20 世纪下半叶问世的合成塑料也才是一种透明的固体材料。除了玻璃之外透明的固体材料极少。宝石或半宝石通常是有颜色的,具有一定的透明度(图6)。金属、植物和陶瓷通常是不透明的,只有将它们切割打磨成足够薄的薄片时它们才是透明的。液体通常是透明的,例如水。但在特定条件下液体也会变得不透明了,如凝固后的油。

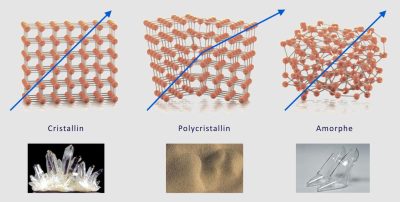
透明度与材料的原子结构有关。当液体凝固成固体时,可以形成单晶体,并且单晶局部和整体都保持着周期性的有序排列。在空间中有规律地排列的原子或分子形成了晶体。由纯碳有序排列形成的钻石就是典型的单晶。然而,大多数情况下,结晶并不完美,小的单晶体形成并聚集在一起形成固体。这些单晶畴之间的过渡区(称为晶界)是缺陷的一种形式,表明了原子周期性有序排列遭到了改变。原子的排列会影响光在固体中的传播方式,因为光的传播取决于材料的原子结构。在宝石等大块单晶体中,光线在其内部传播是不会受到干扰的,因此它是透明的。相反,在多晶体中,各个小晶体之间取向不同,光线经常遇到晶体取向的变化,会导致光的漫散射和衍射(图7),从而影响了材料的透明度,当光线发生大量的偏离时,材料有时甚至会呈现出白色。
[来源:http://physiquechimiecollege.eklablog.com/etats-de-la-matiere-a100286069, DR]
多晶固体材料熔化后,其周期性的排列就消失了,光的传播就又不受到干扰了,从而使材料变得透明了。由于大块单晶材料稀缺,除玻璃和聚合物外,透明固体非常罕见而且通常尺寸较小,一般来说它们的制备也很困难。就玻璃而言,虽然它是固体,但其无序的结构在所有取向上没有有序排列或缺陷,这就使得它能像液体一样透明。
3.2 玻璃为什么坚固耐用?

玻璃的硬度、机械强度和耐用性均与玻璃材料中硅(Si)和氧(O)之间的化学键特性有关。SiO2分子的化学键特别强,通过连续的三维网状结构将硅原子和氧原子牢固地结合在一起。
化学键的键能决定了玻璃的硬度、机械强度和耐用性。纯的氧化硅晶体,例如石英就是键能强大的典型例子,即使它在高温(超过1600°C)下也不会熔化。

玻璃具有卓越的耐用性,它可以历经千年而不被侵蚀。然而,尽管玻璃具有很高的机械强度,但它耐冲击力低,碰撞时易碎,从而限制了其应用范围。此外,玻璃在温度迅速升高时也容易破碎,这是由于玻璃(绝热材料)的导热性差和热膨胀所引起的。当玻璃加热不均匀时,较高温区就会进一步地膨胀,再加上高温导致的机械应力变化,极易使玻璃破碎。
科学家们已经研发出了强化玻璃,找到了提高玻璃耐热性和机械强度的解决方案。微晶玻璃(图9)就是改善玻璃性能的一个很好的案例,通过受控的部分析晶,微晶玻璃包含分散在玻璃基体中的玻璃微晶,从而大大地降低了热膨胀系数。在力学性能方面,当可淬火玻璃加热到一定等温度后经过快速冷却,在玻璃表面产生压应力,从而增强了其抗冲击性。
硅和氧形成强化学键,因此玻璃可以耐受化学物质侵蚀,所以通常用于实验室中安全地盛放、混合化学品或进行化学反应。玻璃的这种惰性也使其成为储存食物或盛装香水的理想材料。
此外,玻璃像水一样具有溶解许多离子化合物的能力。二氧化硅 (SiO2)可以转化为硅酸根离子(SiO32-),并与金属阳离子相结合。这就是为什么玻璃能够捕获和溶解多种金属离子的原因:传统配方中的钠离子以及许多其他金属阳离子即是如此。这一特性是许多不同类型玻璃拥有颜色的原因,这种特性也被应用在不同的场景中,例如,将核电站铀裂变产生的核废料与高温熔融的玻璃混合,以便将其固化和封存。
4. 当前研究的前景
4.1 设计创新
尽管玻璃有着悠久的历史,但在这个领域里,无论是材料的新用途还是新工艺,创新仍在探索中。新型玻璃还在不断地涌现,例如硫系玻璃[6]开辟了新的应用前景,尤其是在光学领域里。
如今,专家制造出了令人惊叹的轻薄的柔性玻璃,例如市售的卷筒玻璃纸,玻璃甚至被用作3D打印的基材来制造零部件。显然,玻璃行业未来仍有可挖掘的潜力,未来产品的革新应用还将继续拓宽我们的视野。
4.2 关于玻璃的科学知识仍然不全面
然而,在这段玻璃非凡的发展史中,最令人着迷的依然是围绕着其结构及性质的神秘之处。尽管经过了数千年的使用,玻璃物理结构的基本性质(固态下为非晶结构)仍在引发深入的科学讨论。现代科学将玻璃视为一种与过冷液体类似的非平衡状态的物质,或被认为是物质的一种新的状态。这个谜团持续地激发着研究人员的好奇心,并开辟新的研究视角。因此,玻璃行业仍然是一个令人着迷的领域,需要不断地探索,显然,新的发现和创新将继续提高我们对这种多用途的特殊材料的理解。
5. 谨记于心的信息
- 玻璃是一种独具特色的材料,自古至今应用广泛,并且仍将继续开发出其他各种用途。
- 玻璃具有很多独特的性能,例如透明、坚硬、耐用以及可溶解各种离子化合物。
- 尽管还存在许多其他元素组成,但硅、钠和钙仍然是现代玻璃最常见、最基础的成分。
- 新型玻璃(硫族玻璃)和新外形(极薄的玻璃板、可卷起或可折叠的玻璃片)即将问世。
感谢所有为探索和理解玻璃这一非凡材料做出贡献的人。圣戈班的研发人员、众多合作者和专家功劳赫赫,提升了我们对玻璃的认知。致敬那些保存了有关玻璃的记忆和历史的人们,其中有莫里斯·哈蒙(Maurice Hammon)、玛丽·德·劳比尔(Marie de Laubier)和安妮·阿隆佐(Anne Alonzo)。我们还要感谢参与本文校对的工作人员:玛丽·莉丝·鲁克斯(Marie Lise Roux)、帕斯卡·法布尔(Pascale Fabre)和卡特琳娜·兰格莱斯(Catherine Langlais)。
参考资料及说明
封面图片:一栋现代建筑的玻璃立面。[来源:皮克斯贝图库(Pixabay)标号为652234的照片]
[1] 迪迪埃·鲁克斯《玻璃,持久性的材料》,EDP科学出版社,2024年2月
[2] 浮法工艺是由英国皮尔金顿(Pilkington)公司在20世纪60年代研制的一种革新性工艺,采用此工艺,无需打磨和抛光,只需同一工艺流程将熔融的玻璃连续倒进熔融锡上即可生产出平板玻璃。https://www.aerocontact.com/videos/93159-saint-gobain-glass-float-process
[3] 固体的非晶态并不是玻璃所独有的。其他材料也可以制备出非晶态来,例如,某些金属薄片因快速冷却来不及结晶。许多有机材料也是非晶态的,如大多数的聚合物。
[4] “在叙利亚有一个叫腓尼基(Phénicie)的地区,与朱迪亚(Judée)接壤,在卡梅尔山(Carmel)的山脚下有一片名为森德维亚(Cendevia)的沼泽地。据说它是贝卢斯河(Bélus)的源头,流淌了5000步的距离,在托勒密(Ptolemaïs)附近流入大海。河水流速缓慢,并且不适合饮用,但常在此举行宗教仪式。这条很深的河流满是淤泥,只有在海水退去时才能看出它携带了大量的沙子。那时,被海浪反复搅动的沙子与杂质分离并被冲洗干净,人们坚信这些沙子如果没有海水的冲刷将一文不值。采砂的河岸长不过五百步,几个世纪以来这里是唯一产玻璃的地方。据说,一群硝石商人在那里停靠,在河边准备吃的东西。由于找不到石头来架锅,他们就用了船上的硝石。火炙烤着硝石与地面的沙子,人们看到流出了一种不认识的透明液体,这就是玻璃的起源。”
[5] 在各个大洲都或多或少发现过泡碱矿的沉积物,尤其多见于盐碱沙漠地带的土壤层和土壤底层。
[6] 硫系玻璃主要应用于光学领域。它们由硫族元素(硫、硒、碲)组成。硫系玻璃在可见光下是不透明的,因此通常肉眼看上去呈黑色。
环境百科全书由环境和能源百科全书协会出版 (www.a3e.fr),该协会与格勒诺布尔阿尔卑斯大学和格勒诺布尔INP有合同关系,并由法国科学院赞助。
引用这篇文章: ROUX Didier (2025年1月5日), 玻璃:持久性的材料, 环境百科全书,咨询于 2025年4月3日 [在线ISSN 2555-0950]网址: https://www.encyclopedie-environnement.org/zh/physique-zh/le-verre-un-materiau-eternel/.
环境百科全书中的文章是根据知识共享BY-NC-SA许可条款提供的,该许可授权复制的条件是:引用来源,不作商业使用,共享相同的初始条件,并且在每次重复使用或分发时复制知识共享BY-NC-SA许可声明。










