Zoonoses et environnement
PDF
Grippe aviaire, coronavirus, Ebola, maladie de Lyme, variole du singe… mais pourquoi émergent régulièrement ces nouvelles maladies qui nous viennent des animaux, sauvages ou domestiques ? On sait depuis longtemps qu’il existe de nombreux agents infectieux qui peuvent provoquer une maladie aussi bien chez les humains que chez les animaux. Et que dans certains cas, des agents infectieux propres aux animaux peuvent franchir accidentellement leur barrière d’espèce pour infecter des humains, et provoquer une nouvelle maladie, parfois dévastatrice, dans l’espèce humaine. Ce phénomène, très aléatoire et difficile à prévoir, dépend néanmoins de nombreux facteurs, à la fois environnementaux, sociétaux, comportementaux. Quelles sont ces maladies partagées entre les animaux et l’espèce humaine ? D’où proviennent et comment évoluent les microbes qui en sont responsables ? Quels sont les mécanismes de transmission de l’animal à l’humain ? Quels sont les facteurs de risque et comment se préparer au risque zoonotique ? Cet article répond à toutes ces questions.
1. Les zoonoses, maladies partagées

S’il existe des agents infectieux qui ne sont pathogènes que pour l’humain, et d’autres qui ne sont infectieux que pour une espèce ou un nombre limité d’espèces animales, il existe de nombreux agents infectieux qui peuvent provoquer une maladie aussi bien chez les humains que chez les animaux. Le terme de « zoonose », combinaison des mots grecs zoon, animaux, et noson, maladie, désigne ces maladies infectieuses partagées dans des conditions naturelles entre les humains et les animaux, qu’ils soient sauvages, d’élevage, ou de compagnie.
1.1. Préhistoire : l’Homme et la nature, de proie à prédateur
A l’aube de l’humanité, les hominidés sont fragiles. Ils ont de nombreux prédateurs et survivent en se nourrissant essentiellement de charognes et de cueillette. L’invention du feu et des premiers outils de pierre vont aider les hommes à se défendre : l’humain s’organise socialement, se défend contre les agressions, et devient prédateur à son tour. Il s’adapte aux environnements qu’il rencontre et maitrise la chasse d’animaux sauvages (Figure 2). L’évolution de l’humanité est ainsi jalonnée de rencontres entre les hommes et les animaux, et la transmission des micro-organismes infectieux d’une espèce à une autre est permanente.

1.2. Histoire moderne : l’Homme s’éloigne de la nature
Avec l’ère de l’industrialisation, de l’avènement de la technologie, de l’urbanisation rapide et des modes de vie modernes, l’éloignement de l’Homme et de la nature a indiscutablement réduit le risque de contamination par un agent infectieux provenant de la faune sauvage. Par exemple, le contact avec les chauves-souris ou les rats, vecteurs de nombreuses maladies, s’est très fortement réduit à l’époque moderne. A l’inverse, certains animaux voient leur habitat se réduire ou changer du fait de l’activité humaine ou des changements environnementaux (climat, usage des sols, mobilités…), ce qui les oblige à sortir de leur environnement sauvage ou modifier leur comportement, et ainsi se rapprocher des humains. Et de plus en plus d’humains ont des contacts rapprochés avec des animaux de compagnie.
1.3. L’importance des zoonoses
On estime que plus de la moitié des maladies infectieuses humaines trouvent leur origine chez les animaux. Les zoonoses sont responsables chaque année de plus de deux milliards de cas chez les humains, avec parfois un danger de transmission interhumaine directe et d’évolution épidémique voire pandémique de certaines zoonoses. Les fréquences sont inégales : certaines zoonoses sont très courantes, dans de nombreux pays ; d’autres ne sont présentes que dans des aires géographiques spécifiques ; enfin, certaines sont exceptionnelles, même si leurs conséquences épidémiologiques peuvent être importantes (Ebola, SARS-CoV). Les conséquences médicales des zoonoses chez les humains sont d’ailleurs très variables : certaines sont bénignes et facilement curables (téniase…), d’autres peuvent être mortelles (rage, Ebola, etc.). Enfin, les zoonoses entraînent des conséquences importantes pour les animaux eux-mêmes : des espèces sauvages peuvent être mises en danger d’extinction, des écosystèmes peuvent être bouleversés, et les conséquences économiques sur l’élevage peuvent être très importantes, comme c’est le cas par exemple pour la grippe aviaire.
Parmi les nombreuses zoonoses, celles qui sont susceptibles d’évoluer vers une transmission interhumaine sont particulièrement redoutées (Lire Focus Diversité des zoonoses). La population humaine étant naïve (sans immunité acquise spécifique d’agents pathogènes nouveaux) d’un point de vue immunologique face à l’émergence d’un agent infectieux venant du monde animal, les conséquences sanitaires peuvent alors être désastreuses, comme l’histoire récente l’a montré dans le cas des virus de la grippe, des virus à fièvre hémorragique, et des coronavirus.
2. Zoonoses : mécanismes de transmission
Les zoonoses peuvent être causées par différents types d’agent infectieux : des bactéries ou des rickettsies (bactérie intracellulaire obligatoire), des virus, des prions, des parasites, des champignons. La notion de transmissibilité est importante : certaines maladies sont communes aux animaux et aux humains, mais ne se transmettent pas de l’un à l’autre, et ne sont donc pas considérées comme des zoonoses (par exemple, le tétanos). La plupart des maladies qui se transmettent des animaux aux humains ne se transmettent pas (ou très difficilement) entre humains. Seules quelques zoonoses ont eu la capacité de développer une transmission interhumaine.
L’émergence et l’extension d’une zoonose peut ainsi se résumer en plusieurs étapes :
- Le contact entre l’humain et l’animal porteur de l’agent infectieux ;
- La transmission du microbe entre l’animal et l’humain (avec parfois l’intervention d’un hôte intermédiaire ou d’un vecteur) ;
- L’adaptation du microbe du monde animal à l’hôte humain, suivie ou non d’une éventuelle transmission interhumaine.
Ce qui est remarquable dans ce mécanisme, c’est la transgression de la barrière d’espèce c’est-à-dire le passage d’une espèce à une autre : l’agent infectieux doit moduler ou modifier son mode de développement – et donc de survie – pour s’adapter à cette nouvelle espèce. Enfin il faut noter que toutes les pandémies depuis un siècle ont eu l’animal pour origine (Lire Pandémies virales de l’ère moderne).
2.1. Le risque zoonotique
Les facteurs de risque liés à la transgression de la barrière d’espèce sont de deux types : les facteurs sociologiques et environnementaux influençant la probabilité de contact entre humains et animaux, et les facteurs biologiques liés à l’adaptation de l’agent infectieux à un nouvel hôte :
- Pour une majeure partie des microbes, il existe une spécificité plus ou moins stricte pour une espèce sensible à l’infection. Cette spécificité est liée à la pénétration de l’enveloppe (épiderme, muqueuses), à la reconnaissance et la pénétration par le microbe des cellules cibles, et à l’évasion de formes infectantes hors de l’hôte.
- Les contacts avec les animaux sauvages favorisent l’émergence de pathologies infectieuses inédites. Les occasions de ces contacts ont globalement fortement diminué avec le développement, mais elles ont changé de nature : elles sont de plus en plus liées au tourisme, à la déforestation, à la chasse, au trafic d’animaux sauvages.
- Qu’ils soient d’élevage ou de compagnie, les animaux domestiques présentent un risque avéré de transmission zoonotique. Multipliant le risque de contact avec des agents pathogènes qui se trouvent dans le monde sauvage, ils peuvent également agir comme des vecteurs intermédiaires. Au niveau mondial, on estime à plus d’un milliard et demi le nombre d’animaux de compagnie. On dénombre en centaine de milliards le nombre d’animaux d’élevage.
2.2. Transmission directe et transmission indirecte
On distingue deux grands mécanismes de transmission d’un agent pathogène lors d’un contact animal-humain :
- La transmission directe. L’agent infectieux est transmis d’un animal infecté à un hôte sensible (humain ou hôte intermédiaire) par contact avec un produit d’excrétion biologique (salive, sang, urine ou excréments). Le contact peut se faire par voie transcutanée ou sur des lésions de peau, par voie muqueuse (léchage), par voie aérienne (gouttelettes en suspension dans l’air émises par un animal infecté), par voie digestive (aliment infecté), par voie sanguine (morsure) (Figure 3).

- La transmission indirecte. L’agent infectieux est transmis par l’intermédiaire d’un vecteur. Les vecteurs peuvent être de plusieurs types :
- Des vecteurs inertes, comme des matériels contaminés (objets tranchants ou pointus, surfaces), des insectes infestés sur leurs parties tranchantes/piquantes/suceuses, mais qui n’entre pas dans le cycle naturel de reproduction du microbe (ex. la mouche domestique, Musca domestica, connue pour son rôle de vecteur mécanique dans la propagation de maladies infectieuses variées de type shigellose, salmonellose, staphylococcies).

Figure 4. Aedes aegyptii en phase de repas sanguin. Certains moustiques sont vecteurs de maladies virales ou parasitaires (dengue, chickungunya, encéphalite japonaise, fièvre jaune, paludisme…). [Source : photo (c) James Gathany, Domaine public, via Wikimedia Commons - Des vecteurs actifs (moustiques, mouches, acariens, puces, tiques, rongeurs ou autres vertébrés) nécessaires au cycle naturel de l’agent pathogène (multiplication chez le vecteur et transmission) (Figure 4). Les exemples sont multiples : le bacille de la peste et la puce, les Borrelia et les tiques, le virus de la fièvre de Lassa et le rat à mamelles multiples, les arbovirus et les moustiques culicidés ou les acariens. Ces maladies vectorielles présentent des caractéristiques liées à leur vecteur et à leur cycle de transmission.

Figure 5. Le lait de vache cru peut transmettre aux humains la bactérie de la Brucellose (Brucella melitensis) à partir d’un animal infecté. [Source : © Romo Lomo – stock.adobe.com]
- Des vecteurs inertes, comme des matériels contaminés (objets tranchants ou pointus, surfaces), des insectes infestés sur leurs parties tranchantes/piquantes/suceuses, mais qui n’entre pas dans le cycle naturel de reproduction du microbe (ex. la mouche domestique, Musca domestica, connue pour son rôle de vecteur mécanique dans la propagation de maladies infectieuses variées de type shigellose, salmonellose, staphylococcies).
- Transmission via des produits de consommation : elle a lieu lors de la consommation (viande ou chair infestée insuffisamment cuite, lait cru), lors de la consommation de produits contaminés par les excréments d’un animal infecté (fruits, légumes, céréales), ou lors de la manipulation de produits animaux infectés (dépeçage, transport, préparation) (Figure 5).
2.3. L’émergence des zoonoses
Les émergences de zoonoses sont des évènements rares, difficiles à prévoir dans le temps et dans l’espace, mais leur probabilité augmente dès que l’on considère le risque sur le temps long. Certains facteurs, biologiques, sociaux, environnementaux, comportementaux, en augmentent la probabilité.
2.3.1. Les facteurs de risque d’émergence
L’émergence et l’extension d’une zoonose résultent d’évènements impliquant de multiples facteurs :
- Facteurs liés à la probabilité de rencontre entre animaux et humains ;
- Faculté de mutations biologiques de l’agent pathogène pour la transgression de la barrière d’espèce et l’adaptation à un nouvel hôte ;
- Conditions environnementales et comportementales favorables aux processus de transmission et aux éventuels vecteurs.
La transgression de la barrière d’espèce est le principal mécanisme d’émergence d’une zoonose. Deux évènements essentiels sont nécessaires à ce mécanisme :
- La rencontre de deux espèces et l’échange de microbes : c’est le débordement d’espèce, plus connu dans la littérature sous le terme anglais de « Spillover ».
- La survie du microbe chez l’espèce qui le reçoit : si l’espèce ne le multiplie pas ou le rejette, l’échange n’aboutit pas et l’épisode se termine avec la disparition de l’individu infecté. Si l’espèce receveuse multiplie le microbe, il y a alors transgression de la barrière d’espèce et possible émergence d’une zoonose.
Le mécanisme de passage inter-espèces de l’agent pathogène est sous-tendu par plusieurs facteurs (Figure 6) :

- La plasticité génétique de l’agent pathogène (mutation, recombinaison, réassortiment) qui, pour certains, peut être élevée et leur permet de s’adapter à un nouvel hôte.
- La spécificité d’hôte : certains agents pathogènes ont une faible spécificité d’hôte et peuvent infecter des espèces de taxons proches.
- La pullulation des hôtes vivant en sympatrie (ex. rongeurs, moustiques) peut être un facteur déterminant en favorisant les contacts avec des hôtes vulnérables.
- Des facteurs liés à l’environnement naturel (climat, catastrophes naturelles, etc.) ou d’origine anthropique (densité de population, mobilités humaines et animales, urbanisation, déforestation, fragmentation des espaces naturels, pratiques agricoles et d’élevage, etc.) peuvent favoriser l’émergence, l’extension et l’endémisation d’une zoonose (Lire Changement climatique : quels effets sur notre santé ?).
2.3.2. Des exemples de facteurs de risque d’émergence
2.3.2.1. Facteurs comportementaux
- L’émergence de la maladie de Lyme chez l’humain serait due aux contacts accrus avec les espèces naturellement infectées par la bactérie responsable de la maladie. Aux USA, cerfs et rongeurs, hôtes naturels de la Borrelia transmises par des tiques, se sont mis à proliférer à la suite de régulation de la chasse. Par la suite, le développement d’habitations hors des zones urbaines, plus au contact des lisières forestières, aura probablement contribué à l’émergence de la maladie, puis à son extension dans le nord-est des États-Unis et au Canada.

Figure 7. Les chiroptères (chauves-souris) sont reconnus comme des hôtes, réservoirs et vecteurs de nombreux virus pathogènes pour l’Homme. [Source : montage des auteurs à partir de deux photos ; fond : Grotte avec chauves-souris, El Maviri Sinaloa, Mexique © Tomas Castelazo, www.tomascastelazo.com / Wikimedia Commons – au premier plan Rousettus aegyptiacus, Original photo: אורן פלס Oren Peles Derivative work: User:MathKnight, Licence CC BY 2.5, via Wikimedia Commons] - Fièvres Ebola. En Afrique centrale, certaines espèces de chauves-souris pourraient être infectées de façon chronique par le virus Ebola et en être le réservoir naturel (Figure 7). Des animaux sauvages sensibles à l’infection par le virus (primates, ongulés sauvages) peuvent s’infecter au contact de ce réservoir ou de ses produits biologiques infectés. La contamination humaine pourrait être liée à l’exposition dans la forêt (chasse, dépeçage d’animaux sauvages). La diffusion interhumaine implique d’autres facteurs, liés aux habitudes alimentaires (consommation de viande brousse) et aux comportements sociaux (pratiques rituelles ou religieuses, notamment lors des cérémonies funéraires).
- La variole du singe (ou Monkeypox). De nombreuses espèces de primates et de rongeurs ont été trouvées porteuses du virus. La maladie est transmissible à l’humain et présente des symptômes similaires à ceux de la variole, mais avec une gravité moindre (Lire focus De la variole au Mpox : une menace renouvelée). En mai 2022, des cas de variole du singe ont été reportés à l’OMS par des États non endémiques pour le virus, et ont suivi plus de 62 000 cas dans 105 pays et territoires, avec 23 décès. Heureusement, le vaccin historique de la variole, dont de nombreuses doses sont toujours conservées, s’est avéré efficace contre la variole du singe et a permis l’arrêt de cette pandémie.
- La Cryptosporidiose est une maladie cosmopolite qui se manifeste par une diarrhée sévère chez les animaux (bovins, oiseaux) et les humains. La transmission se fait principalement au contact de l’environnement souillé par les excréments d’animaux contaminés, via l’environnement (cours d’eau, pâturages, jardins) ou par contact direct avec les animaux par voie fécale-orale. Entre 2001 et 2010, le Cryptosporidiose a été la principale cause de maladies liées aux eaux de loisirs aux États-Unis.
- L’Échinococcose alvéolaire est une maladie parasitaire grave causée par le développement de larves du ténia Echinococcus multilocularis chez l’humain. Le parasite est présent chez le chien, le renard, et d’autres carnivores sauvages. Les humains peuvent contracter la maladie par contamination alimentaire en ingérant accidentellement des œufs du parasite présents dans l’environnement (par exemple, sur des baies sauvages). L’échinococcose alvéolaire se caractérise par une période d’incubation asymptomatique de 5 à 15 ans et le lent développement d’une lésion tumorale localisée dans le foie, accompagné de perte de poids, douleurs abdominales, malaise généralisé et insuffisance hépatique. Non traitée, l’échinococcose alvéolaire est mortelle.
- Méningo-encéphalite verno-estivale (MVE). Les saisons peuvent influencer la transmission de certaines zoonoses. Par exemple, les activités de plein air comme le camping et la randonnée augmentent le risque de contact avec les tiques. La MVE est une maladie provoquée par un Flavivirus transmis par la piqûre d’une tique de rongeur infectée, abondante en été.
2.3.2.2. Vulnérabilité sociale et pauvreté
Les zoonoses sont souvent liées à la pauvreté et aux facteurs de vulnérabilité qui en découlent : conditions de vie précaires, systèmes de santé fragiles, accès limité à l’eau potable et à l’assainissement, contacts étroits avec les animaux d’élevage.
- La maladie de Chagas, ou trypanosomiase américaine. D’après les estimations, 6 à 7 millions de personnes dans le monde sont infectées par Trypanosoma cruzi, le parasite responsable de la maladie. Elle se transmet principalement par voie vectorielle, à la suite d’un contact avec des selles ou de l’urine de triatome (variété de punaises) infectés par T. cruzi, ainsi que par voie orale (transmission alimentaire), par le sang et les produits sanguins, ou de la mère à l’enfant (transmission congénitale). Le contact avec les triatomes est fortement lié à la vulnérabilité socio-économique des populations et aux conditions d’hygiène des habitats. La maladie sévit principalement en Amérique latine.
- La Leptospirose. Maladie transmise par les bactéries du genre Leptospira, qui se trouvent généralement dans l’urine des rongeurs. Les personnes vivant dans des zones d’habitat précaire ou insalubre (mauvais assainissement, risque d’inondation, environnement en contact avec des rongeurs) sont plus exposées à cette maladie.
- La Fièvre de la Vallée du Rift. Cette maladie du bétail en zone tropicale est causée par un virus transmis par des moustiques. Les éleveurs peuvent s’infecter par contact avec le sang ou les tissus d’animaux infectés. Les populations qui vivent en milieu rural et qui dépendent de l’agriculture ou de l’élevage sont particulièrement exposées.
- La Leishmaniose, due à des parasites protozoaires appartenant à plus de vingt espèces de Leishmania, est transmise par les piqûres de phlébotomes (mouches de sable). Les populations défavorisées vivant dans des régions d’enzootie avec des conditions de logement précaires sont à risque accrus d’exposition aux piqûres de phlébotomes infectés. On estime de 700 000 à 1 million les nouveaux cas chaque année.
2.3.2.3. Promiscuité avec les animaux domestiques
- Toxocarose et animaux de compagnie. La toxocarose humaine (fièvre, douleurs abdominales, syndrome respiratoire) est une infection parasitaire causée par les larves de vers ronds (Toxocara canis ou Toxocara cati) qui a lieu après ingestion accidentelle des œufs de ces parasites intestinaux des chiens et des chats. Les œufs sont abondants dans les excréments des chats ou des chiens infectés (200 000 œufs par jour par ver parasite), et la transmission chez les humains se fait généralement par l’intermédiaire d’objets, de surfaces, d’aliments souillés ou d’eau contaminée par les œufs. Les mouches peuvent également propager les œufs sur les surfaces ou les aliments.
- Échinococcose kystique des bergers. L’échinococcose kystique est une zoonose cosmopolite causée par une infection du stade larvaire d’Echinococcus granulosus (Ténia) qui infecte les chiens. Le mode de transmission à l’humain est la consommation accidentelle d’eau ou d’aliments contaminés par les matières fécales de chien infecté.
2.3.2.4. Facteurs climatiques et environnementaux
- Maladies vectorielles. Les maladies transmises par des vecteurs, en particulier les moustiques (comme le paludisme, ou de nombreuses arboviroses comme la dengue, le chikungunya, l’encéphalite à virus West Nile, l’encéphalite japonaise, la maladie à virus Zika…) ou les tiques (comme la maladie de Lyme ou l’encéphalite à tique) sont dépendantes de l’abondance et de l’activité de ces vecteurs. Le risque de transmission des maladies vectorielles est accru lorsque les conditions climatiques sont favorables aux vecteurs.

Figure 8. Des oiseaux migrateurs en formation peuvent être vecteurs et réservoirs de nombreuse zoonoses virales [Source : photo licence CC0, via PxHere]: - Comportement animal saisonnier. Certaines maladies zoonotiques présentent des pics saisonniers en raison du comportement animal lié aux facteurs climatiques. Par exemple, le risque lié à la leptospirose est accru pendant la saison des pluies, lorsque les rongeurs infectés quittent les zones inondées ou que des inondations peuvent diffuser des bactéries. Les migrations saisonnières d’animaux peuvent influencer la propagation de zoonoses : les oiseaux migrateurs (Figure 8) peuvent transporter des virus sur de longues distances ; le virus de la fièvre de la vallée du Rift est transporté par le bétail transhumant dans les pays du Sahel en saison sèche à la recherche de pâturage et de points d’eau.
- Pratiques agricoles saisonnière. Dans les régions où l’agriculture est saisonnière, les périodes de récolte peuvent être associées à un risque accru de maladies zoonotiques lié à l’utilisation d’animaux d’élevage mis au contact d’animaux sauvages. Par exemple, la fièvre hémorragique de Junin en Argentine, dont les manifestations épidémiques correspondent à la récolte du maïs et au contact avec les rongeurs des champs infectes par le virus ; le caractère saisonnier de la fièvre jaune au Brésil dont l’incidence augmente au moment de la récolte ou de la plantation du riz et du soja.
- Nipah virus et El Niño. Dus à une sécheresse exceptionnelle, à la déforestation et à une température anormalement élevée provoquée par le phénomène El Niño, d’immenses incendies de forêt à Sumatra ont forcé la migration de chauves-souris depuis Sumatra vers la péninsule Malaise. Des chauves-souris infectées ont introduit un virus inconnu dans la région agricole de Nipah, où il a été identifié pour la première fois. Des animaux d’élevage ont été infectés par les fruits souillés par les chauves-souris en quête de ressources alimentaires.
- La borréliose et la sahélisation des écosystèmes de forêts-savanes en Afrique de l’Ouest. La borréliose africaine, ou fièvre récurrente à tiques, est une maladie grave avec des complications méningo-encéphalitiques. Des petits mammifères sauvages servent de réservoir à la borrélie responsable et l’humain peut être infecté par la piqure de la tique vectrice. Les variations climatiques de la région subsahélienne ont provoqué une extension de la distribution géographique de la tique. La borréliose africaine à tique a désormais une incidence élevée en zone de savane soudanienne (sud de sa zone enzootique historique) où elle était jusque-là absente.
2.1.2.5. Risque alimentaire
- Parasites de la viande. La Sarcocystose intestinale ou musculaire est due principalement à l’Ingestion de kystes de Sarcocystis hominis (protozoaire parasite de bovidés) ou Sarcocystis suihominis (protozoaire parasite de porcins) contenus dans la viande de consommation. La Trichinellose (T. britovi, T. spiralis, etc.) est quant à elle due à la consommation de la viande crue ou peu cuite, préparée à partir d’animaux infectés, tels que le porc, le sanglier, l’ours sauvage. La Téniase est contractée par l’ingestion de cysticerques contenus dans la viande de porc (Taenia solium) ou de bœuf (T. saginata) insuffisamment cuite. L’ingestion d’œuf de T. solium par transmission oro-fécale interhumaine peut aboutir à la Cysticercose.
- Les salmonelloses sont des zoonoses dues à des bactéries qui vivent dans le tractus intestinal de nombreux mammifères et oiseaux. Chaque année, Salmonella est à l’origine de plusieurs centaines de millions d’infections dans le monde, avec plus de 150 000 décès. 85 % des infections sont liées à l’alimentation. Le risque est lié au contact avec les animaux ou les produits contaminés par leurs déjections, et les habitudes alimentaires à consommer des produits crus ou insuffisamment cuits.
- La brucellose est une maladie infectieuse causée par une variété de bactéries du genre Brucella qui infectent principalement les moutons, les bovins, les porcs, les chèvres et les chiens. Les humains peuvent contracter la maladie lors de contacts avec des animaux infectés, en buvant ou consommant des produits d’origine animale contaminés par la bactérie (principalement lait cru ou produits laitiers non pasteurisés), ou encore par inhalation de particules contaminées. La transmission interhumaine est rare.

Figure 9. Filet de saumon du Pacifique (Oncorhynchus keta) présentant un nématode parasite vivant (Anisakis sp.). [Source : photo © Togabi, licence CC0, via Wikimedia Commons] - L’anisakiase et produits de la mer. L’anisakiase est une maladie provoquée par des vers nématodes (ex. Anisakis, Pseudoterranova spp.) qui infectent les poissons (Figure 9) et les mammifères marins, et parfois d’autres organismes marins comme calmars et poulpes. L’infection se produit par la consommation de poissons ou des fruits de mer infectés par des larves d’Anisakis, mangés crus, insuffisamment cuits ou marinés (ex. sushis ou ceviche). L’anisakiase se manifeste par des douleurs abdominales intenses, nausées, vomissements et diarrhées, avec dans certains cas des réactions allergiques.
3. Santé publique : analyse et prévention du risque zoonotique
3.1. L’approche systémique en santé
Pendant longtemps, l’étude des maladies humaines s’est limitée à la recherche de solutions thérapeutiques et de soins, loin d’une vision « santé publique ». Depuis le début du XXe siècle, une approche beaucoup plus large s’est développée dans la foulée des avancées scientifiques de la microbiologie, de l’épidémiologie et des statistiques. Le décryptage d’un état de santé ne fait plus seulement appel aux caractéristiques de l’agent pathogène et de l’individu, mais également à ceux de la population à laquelle il appartient et aux caractéristiques de son environnement, naturel, social, culturel. Ces paramètres concernent notamment les relations des individus entre eux (proximité, contacts, comportements…), les relations avec les autres êtres vivants dans le monde animal ou végétal, et l’exposition à leurs environnements (« One Health »).
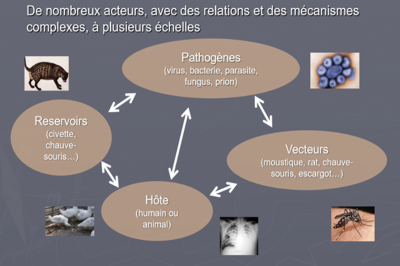
L’approche systémique en santé considère ainsi un phénomène de santé comme un système complexe constitué d’« agents » actifs qui agissent et interagissent en fonction de leurs caractéristiques individuelles et collectives, et d’ environnements auxquels ils sont exposés (Figure 10).
L’approche systémique permet d’aborder l’étude des zoonoses avec la prise en compte de l’ensemble des paramètres nécessaires à la compréhension du phénomène étudié.
3.2. Le risque : conjonction d’aléas, d’exposition à l’aléa, et de vulnérabilités
Dans une approche « santé publique », on peut aborder ce cadre systémique avec une optique « risque », en séparant ce qui est du ressort de la menace et ce qui est du ressort de la vulnérabilité (c’est-à-dire l’aptitude à être plus ou moins affecté par une menace) :
- La menace (ou « aléa ») peut être la présence d’un agent pathogène, d’un vecteur, d’un réservoir, de polluants, de substances nocives, bruit, présence industrielle à risque, etc.
- La susceptibilité de l’individu (essentiellement due aux caractères individuels, génétiques et biologiques -tel le statut immunitaire, ou l’âge) est fortement liée à la pathologie.
- La vulnérabilité « passive » de l’individu, qui ne dépend pas forcément de la pathologie mais qui peut influencer l’exposition de l’individu à la menace ou sa protection à la pathologie.
- La vulnérabilité « active », qui comprend tous les facteurs qui sont susceptibles d’augmenter l’exposition directe de l’individu à la menace.
3.3. Zoonoses et santé publique
Cette approche pragmatique est particulièrement adaptée à l’étude du risque zoonotique. Elle différencie :
- ce qui est de l’ordre de la menace biologique naturelle, souvent sujette à une forte variabilité aléatoire dans le temps et dans l’espace (certains événements de faible voire très faible probabilité doivent parfois être pris en compte, comme l’émergence d’un agent pathogène venant du monde animal, bien souvent impossible à prévoir ou à contrôler) ;
- de ce qui est de l’ordre de la vulnérabilité, en général beaucoup plus stable au niveau des populations humaines ou des infrastructures, et qui permet une meilleure action en santé publique.
On parle ainsi de préparation plutôt que de prévision, et encore moins de prédiction. Cette démarche permet également d’appréhender de façon rationnelle les situations de crise :
- d’une part en ciblant de façon préventive les éléments les plus importants ou les plus fragiles du système, en termes de vulnérabilité (les enjeux, comme par exemple le système de santé) ;
- d’autre part en optimisant la gestion et les actions visant à réduire dans l’urgence la menace (élimination de vecteurs, isolements, abattages d’animaux infectés, etc.) ou la susceptibilité et l’exposition de la population (vaccinations, hygiène, protection, quarantaines, confinements…).
4. Messages à retenir
- Les zoonoses, maladies d’origine animale, restent un danger majeur pour la santé humaine : plus des deux-tiers des maladies infectieuses qui émergent actuellement proviennent de la faune sauvage ou domestique.
- Il est impossible d’éradiquer les agents pathogènes qui sont maintenus dans l’environnement par la faune sauvage. Réduire la susceptibilité de la faune sauvage ou des animaux d’élevage à un agent pathogène en particulier par la vaccination est parfois possible, mais avec une efficacité toujours assez faible.
- Dans le cas de maladies transmises par des insectes (moustiques, tiques, punaises…), on peut tenter d’éradiquer l’agent pathogène par la lutte antivectorielle, mais c’est un combat souvent difficile.
- Se préparer au risque d’émergence et de diffusion de zoonoses est essentiel, surtout lorsque l’émergence peut être suivie de diffusion interhumaine pouvant conduire à des évènements épidémiques ou pandémiques. La préparation au risque concerne essentiellement la vulnérabilité des populations humaines et animales (élevages et domestiques) : pratiques d’hygiène, comportements, habitudes alimentaires, exposition aux vecteurs (moustiquaires), pratiques agricoles, biosécurité des élevages.
- Pour éviter le risque épidémique voire pandémique lorsqu’une transmission interhumaine directe apparait après transgression de la barrière d’espèce de l’animal à l’humain, la préparation implique la mise en place de systèmes de surveillance et d’alerte rapide afin de limiter la diffusion de l’agent infectieux avant qu’elle ne devienne incontrôlable.
- La préparation au risque d’épidémie implique également l’élaboration de plans de gestion de crise, avec la préparation du système de santé pour éviter son engorgement et la pénurie de matériel ou de médicaments, ainsi que des mesures de réduction de l’exposition des populations à l’agent pathogène si nécessaire.
Notes et références
Image de couverture. Un garçon rentre chez lui avec son troupeau familial au crépuscule dans le village de Lhate, à Chokwe, au Mozambique, où circulent de nombreux virus zoonotiques dont le Virus de la fièvre de la Vallée du Rift. [Source photo : © ILRI/Stevie Mann, licence CC BY-NC-ND 2.0 Deed].
L’Encyclopédie de l’environnement est publiée par l’Association des Encyclopédies de l’Environnement et de l’Énergie (www.a3e.fr), contractuellement liée à l’université Grenoble Alpes et à Grenoble INP, et parrainée par l’Académie des sciences.
Pour citer cet article : GONZALEZ Jean-Paul, SOURIS Marc (15 septembre 2024), Zoonoses et environnement, Encyclopédie de l’Environnement. Consulté le 10 avril 2025 [en ligne ISSN 2555-0950] url : https://www.encyclopedie-environnement.org/sante/zoonoses-environnement/.
Les articles de l’Encyclopédie de l'environnement sont mis à disposition selon les termes de la licence Creative Commons BY-NC-SA qui autorise la reproduction sous réserve de : citer la source, ne pas en faire une utilisation commerciale, partager des conditions initiales à l’identique, reproduire à chaque réutilisation ou distribution la mention de cette licence Creative Commons BY-NC-SA.







