Il était une fois la vie : la chimie dans l’océan terrestre il y a 4 milliards d’années
PDF
Il y a quelque 4 milliards d’années, la Terre était largement recouverte par un immense océan. Cet océan contenait un grand nombre de petites molécules organiques, que l’on dit « prébiotiques » parce qu’elles étaient là avant que la vie n’apparaisse. Quelles étaient-elles ? Furent-elles synthétisées sur place ou sont-elles venues de l’espace ? Comment se sont elles liées pour former de longs polymères, certains porteurs de l’information génétique, d’autres s’activant à reproduire toutes les molécules de base et à les agréger à leur tour en polymères ? Rien n’était gagné d’avance ! Les polymères n’étaient pas stables, les liens étaient difficiles à créer. Pourtant, nous sommes là. C’est donc bien qu’une chimie d’une finesse extrême trouva l’énergie et le temps nécessaire pour se mettre en place. Cet article donne quelques pistes pour tenter de comprendre ce qui a bien pu se passer.
1. Il y a bien longtemps, dans une galaxie pas bien lointaine
Il y a environ 4,6 milliards d’années, en un lieu excentré de la galaxie spirale que nous appelons la Voie lactée, un vaste disque de matière s’est formé. L’essentiel des gaz, des grains, des blocs qui constituaient ce disque s’est concentré, a fusionné, pour former une étoile, le Soleil. Le peu de matière résiduelle qui restait a formé des planètes et des objets plus petits, des planètes naines et astéroïdes. Notre Terre, en fait une proto-Terre, s’est donc formée à ce moment-là. Cinquante millions d’années plus tard (un rien à l’échelle des temps astronomiques) cette proto-Terre a été percutée par un objet très massif, Théia, un planétoïdePetit corps céleste présentant certaines caractéristiques d’une planète. Le terme désigne des structures aussi variées que des astéroïdes, des planètes naines, des protoplanètes, etc. de la taille de Mars. De ce choc gigantesque naquit la Lune et notre Terre actuelle [1].
Avant ce choc, il est probable que l’atmosphère terrestre contenait beaucoup d’hydrogène, le constituant majeur du disque proto-solaire. Mais le choc fut gigantesque. Les éléments légers furent expulsés. Une nouvelle atmosphère en résulta, riche en dioxyde de carbone (CO2), en azote (N2) et en vapeur d’eau (H2O). La Terre était encore très chaude. Elle se refroidit pourtant assez vite. La vapeur d’eau se condensa et tomba en une incessante pluie diluvienne pour former un premier, unique et immense océan.
Sous cet océan, la partie supérieure du manteau terrestre se solidifiait, formant une première croute terrestre. Une première tectonique des plaques se mit peu à peu en place. Peut-être jaillissant de l’océan apercevait-on alors déjà quelques proto-continents, des îles éparses, sûrement des volcans bien plus actifs que nos volcans actuels. Notre planète était encore pleine d’énergie ! Cela compensait la faiblesse du jeune Soleil, plus petit et moins puissant qu’aujourd’hui. Sans l’énergie dégagée par la planète, sans l’important effet de serre conséquence de la proportion élevée de CO2 dans l’atmosphère, il est bien possible que toute l’eau soit devenue glace. Quelle sorte de vie aurait pu naître dans cette glace ? Sans doute, aucune…
De même que la proto-Terre croisa la route de Théia, après la naissance de la Lune, la Terre fut percutée par de nombreux astéroïdes qui lui apportèrent probablement une bonne quantité d’eau supplémentaire, peut-être aussi des molécules organiques. Après un intense rebond de ces bombardements cataclysmiques, ils prirent fin il y a 3,8 milliards d’années (enfin, presque fin : nous ne sommes toujours pas à l’abri d’un choc catastrophique. Ce ne sont pas les dinosaures qui diront le contraire !).
Il n’est pas impossible que la vie soit apparue avant la fin de ce « grand bombardement tardifPériode de l’histoire du système solaire s’étendant approximativement il y a 4,1 à 3,9 milliards d’années, durant laquelle se serait produite une notable augmentation des impacts météoriques ou cométaires sur les planètes telluriques. », mais les preuves en ce sens restent ténues. Et même si elle avait démarré, aurait-elle survécu à ces catastrophes à répétition ? (Lire L’origine de la vie vue par un géologue qui aime l’astronomie).
2. Que d’eau ! Que d’eau !
Plaçons-nous donc, il y a un peu moins de 4 milliards d’années, à une époque géologique qu’on appelle l’Hadéen. A cette époque, la Terre comporte un gigantesque océan, des volcans hyperactifs, des embryons de continents. La Lune s’en écarte, mais elle est loin d’avoir atteint son orbite actuelle : elle est encore trois fois plus proche. En conséquence, la force des marées est gigantesque, plus de vingt fois supérieure à ce qu’elle est aujourd’hui. Les vents sont impressionnants. Même si il est en cours de refroidissement, la température de l’océan est sans doute plus chaude que de nos jours.
Il est difficile de connaître son pHAbréviation pour Potentiel d’Hydrogène, une mesure de l’activité de l’ion hydrogène (ou proton) dans une solution. Le pH est un indicateur de l’acidité (pH inférieur à 7) ou de l’alcalinité (pH supérieur à 7) d’une solution. Une solution de pH 7 est dite neutre. : il est actuellement légèrement basique (vers 8,1) mais il s’acidifie à cause des émissions de CO2 d’origine humaine. Dans l’eau, le CO2 forme en effet un acide : l’acide carbonique. Il y a aujourd’hui beaucoup moins de CO2 dans l’atmosphère qu’à l’époque où naissait la vie. Peut-être l’océan était-il donc alors plutôt acide, ce qui n’est pas sans conséquence sur la chimie qui pouvait s’y produire. Il contenait bien sûr des ions. Comme aujourd’hui le sodium (Na+) et les chlorures (Cl–) dominaient. L’océan était déjà salé ! Il y avait aussi du calcium, du magnésium, des bromures, et même bien plus d’iodures qu’aujourd’hui.
On a d’abord pensé que l’atmosphère primitive était très réductrice, qu’elle contenait beaucoup d’hydrogène, de méthane, d’ammoniac. Mais nous l’avons vu, si hydrogène il y avait eu, le choc avec Théia entraina l’expulsion vers l’espace de ce gaz léger. Pour autant l’atmosphère n’était pas oxydante. Elle ne contenait pas, ou presque pas, d’oxygène moléculaire (O2). On parvient à dater l’apparition d’une quantité significative d’O2 sur Terre en déterminant l’âge des plus anciens gisements contenant du fer ferrique. En effet, lorsque l’on expose du fer à de l’eau contenant de l’oxygène, il rouille. C’est-à-dire qu’il est oxydé en fer ferrique (Fe3+). Le fer ferrique n’est pas soluble dans l’eau. Sans oxygène par contre, le fer forme des ions ferreux (Fe2+) qui eux sont solubles.
Il y a donc une différence majeure entre notre océan actuel et l’océan Hadéen : celui-ci contenait du fer ferreux dissout, pas le nôtre.
3. Une foultitude de petites molécules

Cet océan contenait aussi des molécules organiques. A partir de CO2 ou de méthane (CH4), des molécules comportant deux atomes de carbone se forment aisément. Le CO2 peut être réduit en formaldéhyde (H2CO, Figure 1) qui par une réaction qu’on appelle « réaction de formoseMot formé par la contraction des termes formaldéhyde et aldose. Cette réaction, découverte par le chimiste russe Alexandre Boutlerov en 1861, consiste à polymériser le formaldéhyde pour former des sucres y compris des pentoses (sucres à cinq atomes de carbone). Cette réaction est importante dans les processus de formation abiotique des molécules du vivant. » donne d’abord l’hydroxyacétaldéhydeMolécule de structure chimique C2H4O2. C’est la molécule la plus simple qui possède à la fois un groupement hydroxyle (OH) et un groupement aldéhyde (CHO). (une molécule à deux carbones) puis des molécules plus longues qui sont des sucres. Un cuisinier dirait qu’avec ces sucres en plus du chlorure de sodium, l’océan hadéen était sucré-salé !
En plus des sucres, il faut au moins deux types de molécules pour construire une cellule vivante : des protéines et des acides nucléiques. Ces molécules contiennent toutes de l’azote. Quelles pouvaient être les sources de cet azote dans l’océan prébiotique ? Sans doute l’ammoniac (NH3), et l’acide cyanhydrique (HCN). Lorsque ces deux composés réagissent avec le formaldéhyde ils donnent le plus simple des aminoacides, la glycine. Cette molécule est synthétisée grâce à une réaction essentielle qu’on appelle synthèse de Strecker, du nom d’Adolph Strecker, chimiste germanique, qui l’a découverte au milieu du XIXe siècle. Cette synthèse, à partir d’autres aldéhydes, peut donner divers aminoacides, par exemple la sérine à partir de l’hydroxyacétaldéhyde (Figure 1).
Ces aminoacides sont les constituants de base des polymères que sont les protéines. Comme nous venons de le voir, ils ont pu être synthétisés assez facilement : ils étaient donc très probablement présents dans l’océan primitif.
Quid des précurseurs des acides nucléiques, ADNAbréviation pour acide désoxyribonucléique. L’ADN est une macromolécule constituée de monomères nucléotidiques formés d’une base azotée (adénine, cytosine, guanine ou thymine) liée au désoxyribose, lui-même lié à un groupe phosphate. C’est un acide nucléique, au même titre que l’acide ribonucléique (ARN). Présent dans toutes les cellules ainsi que chez de nombreux virus, l’ADN contient l’information génétique, appelée génome, permettant le développement, le fonctionnement et la reproduction des êtres vivants. Les molécules d’ADN des cellules vivantes sont formées de deux brins antiparallèles enroulés l’un autour de l’autre pour former une double hélice. et ARNAbréviation pour acide ribonucléique L’ARN est une macromolécule constituée d’un enchaînement de ribonucléotides (adénine, cytosine, guanine, uracile) reliés entre eux par des liaisons nucléotidiques et exerçant de nombreuses fonctions au sein de la cellule. C’est un acide nucléique, au même titre que l’ADN., qui portent l’information génétique ? Leur synthèse est un peu plus complexe. Il est moins évident que tous aient été présents. Mais il est possible d’écrire des synthèses prébiotiques pour chacun d’entre eux. Le riboseLe ribose est un ose (sucre) constitué d’une chaîne de cinq éléments carbone ainsi que d’une fonction aldéhyde. C’est un composant de l’ARN utilisé dans la transcription génétique. Il est apparenté au désoxyribose qui est un composant de l’ADN. Il est également présent dans de nombreuses molécules importantes dans les processus métaboliques (en particulier l’ATP ou adénosine triphosphate). peut ainsi être obtenu par la réaction formose déjà citée, les bases nucléiques à partir de l’acide cyanhydrique, et des voix d’accès directes aux ensembles ribose-base ont récemment été publiées par les chercheurs.
La synthèse des chaines d’ADN et ARN pose néanmoins la question de la source de phosphore. Il est en effet abondamment présent dans ces polymères porteurs de l’information génétique. Dans notre monde oxydantEn chimie, un élément chimique est oxydant lorsqu’il donne un ou plusieurs électrons lors d’une réaction d’oxydoréduction (voir aussi oxydoréduction et réducteur dans le glossaire)., on trouve généralement cet élément sous la forme de phosphate, en particulier du phosphate de calcium, insoluble dans l’eau. Y avait-il des phosphates (solubles) dans l’océan hadéen, pour le moins non-oxydant ? Sinon, quelle était la source de phosphore soluble ? C’est une question non tranchée [2].
Autre élément important : le soufre présent aujourd’hui dans deux aminoacides indispensables à la vie, la méthionine et la cystéine. Il s’en dégage des quantités importantes des volcans actifs, des fumeroles, de nombreuses sources hydrothermales, souvent sous forme d’hydrogène sulfuré (H2S). Il est donc raisonnable de penser que l’océan primitif contenait de l’hydrogène sulfuré, et par voix de conséquence, de petites molécules sulfurées, par exemple un aminoacide, la cystéine.
Si nous sommes certains (d’aucun diront : à peu près certains) que jamais aucun petit homme vert venu de l’espace intergalactique, n’a posé le pied sur notre planète, il n’est pas impossible que certaines des molécules citées ici aient atterri, ou plutôt amerri, sur Terre, apportées par les millions d’astéroïdes qui l’ont frappée, en particulier pendant le grand bombardement tardif. Ainsi, la magnifique visite qu’a rendue la sonde Rosetta à l’astéroïde 67P/Tchourioumov-Guérassimenko, dit « Tchouri », a montré que celui-ci contenait de l’eau, de l’ammoniac, du formaldéhyde, de l’acide cyanhydrique, de l’hydrogène sulfuré… mais aussi des molécules organiques plus complexes parmi lesquelles la glycine, ce petit aminoacide dont nous avons décrit plus haut une synthèse possible sur Terre (Lire Comment étudier les molécules organiques des comètes ?).
Alors la première glycine : « terrestre » ou « extra-terrestre » ? Et les autres aminoacides ? Et les bases de l’ADN ? Personne n’en sait rien. Mais ce qui est certain c’est que lorsque les bombardements massifs ce sont arrêtés, lorsque cette éventuelle source extra-terrestre s’est tarie, que toutes ces molécules extra-terrestres ont été utilisées, il a bien fallu que des synthèses terrestres prennent le relais. Comme nous l’avons vu, elles sont tout-à-fait possibles. L’hypothèse extra-terrestre, si elle ne peut être réfutée, n’est pas indispensable pour décrire la naissance de la vie sur Terre.
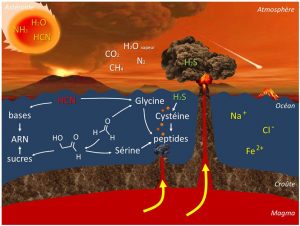
La Figure 2 résume toute cette chimie.
Reste le problème de la concentration de ces molécules. C’est une question très importante : plus les composés de départ d’une réaction donnée sont dilués plus la réaction est lente. Certes la vie avait le temps devant elle. Sauf que beaucoup de produits résultants de la condensation des petites molécules sont peu stables dans l’eau. Il faut pouvoir en faire assez, assez vite, pour qu’elles continuent à grandir, à former des molécules de plus en plus longues, de plus en plus complexes, avant de se séparer à nouveau en petits constituants de départ. Cela pose deux questions : Quelle était la quantité d’eau présente sur Terre ? Et cette eau, quelle masse de molécules organiques contenait-elle ?
Combien d’eau ? L’hypothèse la plus réaliste est de considérer qu’il n’y en avait, grosso modo, ni plus ni moins qu’aujourd’hui, c’est à dire environ 1,36 milliard de km3, soit en arrondissant mille milliards de milliards de litres, ce qui n’est pas rien !
Savoir combien il y avait de molécules organiques, en chemin vers la vie, est bien plus compliqué. La biosphère terrestre actuelle comporte 2 000 gigatonnes (2 000 milliards de tonnes = 2 milliards de milliards de grammes) de carbone organique. Il est très improbable qu’il y en ait eu plus, sous forme de petites molécules, à un moment où la vie justement « organique » n’était pas encore apparue.
Faisons le calcul : 2 milliards de milliards de grammes divisé par mille milliards de milliards litres, cela fait 2 milligrammes de carbone organique par litre d’eau. C’est une concentration faible, sans être totalement ridicule. Mais elle ne donne qu’une idée sans doute surestimée de la concentration en molécules organiques dans l’océan hadéen. La concentration réelle était sans doute encore plus faible. Alors ? Comment envisager des réactions assez rapides dans cet océan brassé continument par des marées gigantesques, et donc grossièrement homogène ?
Darwin lui-même avait déjà exprimé le problème lorsqu’il écrivait à son ami Joseph Hooker, en 1871 :« Mais si (et oh, quel énorme si), nous pouvions concevoir dans une petite mare chaude contenant toutes sortes de sels d’ammoniac et de sels phosphoriques, avec de la lumière, de la chaleur, de l’électricité, etc., qu’un composé protéique fut formé chimiquement, prêt à subir des changements encore plus complexes … »
C’est l’origine de cette petite mare chaude, « warm little pond », qui a proprement fait fantasmer tant de chercheurs à la recherche des origines de la vie. Darwin sous-entend que sa petite mare est assez concentrée pour que la chimie y avance jusqu’à la synthèse d’une chaine assez longue d’aminoacides, le « composé protéique ».
Il y avait peut-être de petites étendues d’eau sur les continents naissants de l’Hadéen, mais les molécules organiques y étaient-elles plus concentrées que dans l’océan global ? Peut-être des molécules se concentrèrent-elles sur les premières plages, ou dans quelques fissures ? Y avait-il plus de composés organiques autour des volcans ? Ou au fond de l’océan, près des cheminées hydrothermales dont s’échappent des volutes de gaz chauds ? Ne faut-il pas plutôt imaginer des réactions particulièrement efficaces permettant de construire des polymères (des protéines, par exemple) même dans des conditions très diluées ?
4. Les clés de la réussite : énergie et catalyse
Pour qu’une réaction chimique ait lieu, il faut :
- qu’elle soit possible, c’est une question de thermodynamique,
- quelle soit assez rapide, c’est une question de cinétiqueEn chimie, la cinétique décrit l’évolution des systèmes chimiques dans le temps, c’est-à-dire le passage d’un état initial à un état final. Les lois de la cinétique chimique permettent de déterminer la vitesse propre à une réaction chimique..
Or, a priori, il y a 4 milliards d’années, rien n’allait de soit !

D’un point de vue thermodynamique ce qui importe c’est la stabilité relative des molécules présentes et des molécules formées. Construire un polymère se fait pas à pas. D’abord deux monomèresConstituants de base de molécules complexes (protéines, sucres complexes, acides nucléiques, etc.). L’enchaînement successif de ces molécules (identiques ou différentes), donne naissance à une structure polymère. Ainsi les acides aminés forment des protéines, les oses forment des sucres complexes, les nucléotides forment des acides nucléiques. donnent un dimère, qui sera allongé en trimère et ainsi de suite jusqu’à des chaines très longues. Au début donc, deux monomères forment un dimère en éliminant de l’eau. Que ce soit dans le cas des peptides (Figure 3) ou dans celui des acides nucléiques, les dimères sont bien moins stables que les monomères. Autrement dit, c’est la réaction de coupure des dimères (une hydrolyse) qui est favorisée. L’équilibre est donc déplacé vers les monomères. Et ce d’autant plus que cette hydrolyse consomme une molécule d’eau, ce qui dans l’eau est favorable, alors que la condensation forme à côté du dimère une molécule d’eau, ce qui est défavorable. C’est ce problème de formation défavorable d’une molécule d’eau qui conduit certains auteurs à chercher les milieux les moins aqueux possibles pour y placer leur scénario d’origine de la vie, les côtes des premiers continents en particulier, où on pouvait sans doute trouver des endroits relativement secs.
Ce n’est pas mieux côté cinétique. Pour que deux molécules réagissent ensemble, il faut les activer, c’est à dire leur fournir une certaine quantité d’énergie. Plus l’énergie à fournir est élevée, plus la probabilité que deux monomères se rencontrent (on parle de « chocs ») sans réagir, est grande. Autrement dit, plus la réaction est lente. Or l’énergie à fournir pour former un dimère embryon de protéine ou d’acide nucléique est grande.
Peine perdue ? Non, puisque malgré tout ça, il est tout à fait certain que la vie est apparue. Pour y arriver, il faut au moins :
- une molécule riche en énergie. En se coupant en deux fragments cette molécule va libérer une bonne partie de l’énergie qu’elle contient. Si cela se passe en même temps que la formation d’un dimère (par exemple un dipeptide), alors les deux énergies vont se compenser et le processus global sera favorisé par la thermodynamique ;
- un catalyseur, c’est à dire une espèce chimique : une molécule, mais aussi parfois la surface d’un solide, (lire Origine des premières cellules : le point de vue de l’ingénieur) capable d’aider la formation d’un dimère à partir de deux monomères. Le nombre de chocs efficaces (ceux formant vraiment le dimère) sera alors bien plus élevé, et la réaction atteindra une vitesse raisonnable dans l’océan prébiotique.

La molécule riche en énergie utilisée aujourd’hui dans les organismes vivants est l’ATP (Figure 4), un triphosphate. La coupure d’une liaison phosphate libère suffisamment d’énergie pour équilibrer l’instabilité des dimères à synthétiser. Dans la synthèse peptidique cela va même permettre d’aboutir au dimère via des intermédiaires encore moins stables que le dimère lui même. On forme dans un premier temps un anhydride mixte carboxylique phosphorique, puis un ester, enfin un amide (le peptide). Au total, cela implique trois étapes, chacune étant intrinsèquement lente. Des catalyseurs entrent donc en jeu. Il en a fallu aussi pour que les tout premiers peptides se forment dans l’océan Hadéen.
Expliquer l’apparition de la vie nécessite donc d’identifier d’une part au moins une source moléculaire d’énergie (sachant qu’il est fort peu probable que l’ATP existât dans l’océan primitif, il est trop riche en énergie), et d’autre part des catalyseurs initiaux (étant entendu que ceux utilisés aujourd’hui dans les cellules vivantes, aminoacyl ARNt synthétasesFamille d’enzymes qui catalysent l’estérification des acides aminés sur l’extrémité 3′ des ARN de transfert (ARNt). Conservées chez tous les organismes vivants, ces enzymes participent à la traduction du message génétique en protéines. Les acides aminés ainsi ajoutés à l’extrémité des ARNt sont ensuite incorporés par le ribosome dans la chaîne polypeptidique (protéine) en cours de synthèse. Il existe une aminoacyl-ARNt synthétase pour chacun des 20 acides aminés présents dans les protéines. Chacune de ces enzymes reconnaît un acide aminé et un ou plusieurs ARNt isoaccepteurs. Leur fonction est essentielle à la fidélité de la traduction du code génétique, car c’est elles qui garantissent que l’acide aminé qui est ainsi estérifié à l’extrémité de l’ARNt correspond bien au bon anticodon. et autres, sont infiniment trop complexes pour être prébiotiques).
Le problème étant posé, tout le reste n’est qu’hypothèse. La plus communément admise aujourd’hui est celle du « monde d’ARN » [3] (lire Origine des premières cellules : le point de vue de l’ingénieur). Elle suppose que les premiers polymères significatifs furent des ARN, à la fois dépositaires de premières informations génétiques et catalyseursÉlément (organique ou minéral) qui accélère ou ralentit une réaction chimique. Utilisé en très petite quantité et spécifique d’une réaction donnée, le catalyseur ne figure pas dans l’équation de la réaction ; il n’influence pas le sens d’évolution de la transformation, ni la composition du système dans l’état final. Une enzyme est un catalyseur biologique.. De fait, certains ARN des cellules vivantes actuelles ont des propriétés catalytiques (même si la très grande majorité des catalyseurs biologiques sont des protéines). En ce qui concerne la source d’énergie : il est impossible de former des ARN sans utiliser l’énergie contenue dans les triphosphates. Or il est peu probable que des triphosphates aient pu exister dans l’océan primitif. C’est une des difficultés de l’hypothèse. Mais elle a l’avantage de concilier information génétique et catalyse.
D’un autre côté, les protéines ne portent pas d’information génétique, mais elles sont de bien meilleurs catalyseurs que les ARN. Cette absence d’information génétique est-elle rédhibitoire pour faire des protéines les premiers polymères vraiment importants dans l’histoire de la vie ? Peut-être pas… Aujourd’hui en effet, certains peptides sont fabriqués directement sur des protéines, sans l’aide d’acides nucléiques. Ces peptides sont dit « non-ribosomaux », parce qu’ils ne sont pas fabriqués dans les ribosomesComplexe composé d’ARN et de protéines ribosomiques, associé à une membrane (au niveau du réticulum endoplasmique granuleux) ou libre dans le cytoplasme. La fonction du ribosome est de traduire le code génétique en protéines, par l’intermédiaire des ARN messagers (ARNm). L’activité enzymatique du ribosome étant portée par les ARNr, le ribosome est un ribozyme. Commun à toutes les cellules (procaryotes et eucaryotes), la structure et la composition du ribosome varie selon les organismes. Chez les procaryotes, le ribosome est dit 70S (S correspondant à l’unité de sédimentation de Sverdberg) et il est constitué des sous-unités 50S et 30S. Le ribosome des eucaryotes est appelé 80S formé des deux sous-unités 60S et 40S., des complexes d’ARN. Pourtant, ils ne sont pas fabriqués « au hasard » et des auteurs ont proposé l’existence d’un code différent du code génétique classique (qui traduit l’ADN en protéines via les ARN). Ce code « non-ribosomal » traduit des protéines en peptides (on pourrait dire des peptides en peptides). C’est un code complexe, basé sur des ensembles de dix aminoacides (dans la protéine codante) : il permet de choisir précisément l’aminoacide à introduire dans le peptide à synthétiser. Rien n’interdit donc d’imaginer qu’une information « pré-génétique », même sommaire, ait pu être portée à l’origine par des chaines d’aminoacides.

Bien que les protéines catalytiques soient des molécules complexes, leur activité repose généralement sur des principes assez simples. C’est le cas des triades catalytiques que l’on retrouve dans des hydrolases et des transférases. Trois aminoacides sont nécessaires : un alcool ou un thiol, une base et un acide. Dans la Figure 5, c’est un thiol, la cystéine, qui agit. Grâce à l’histidine (la base) située plus loin dans la chaine protéique, cette cystéine perd son proton. Elle porte alors une charge négative, ce qui lui permet de réagir avec le carbone positif de la double liaison C=O. L’acide aspartique est là pour activer l’histidine. Le produit de la réaction est, dans ce cas, un thiolester, un autre exemple, après les triphosphates, de molécule à haute énergie. Ce thiolester pourra ensuite subir d’autres réactions, par exemple avec l’eau pour faire un acide (la protéine qui contient la triade est alors une hydrolase), ou avec une autre molécule organique (la triade est le site actif d’une transférase).
Bien sûr, dans nos protéines actuelles, ces triades sont positionnées très précisément par les chaînes d’aminoacides qui les lient. Grâce à cela, chaque protéine à triade est spécialisée et ne réalise qu’un type de réaction sur des molécules elles aussi bien définies. Mais, il y a 4 milliards d’années, dans l’océan terrestre, pouvait-il y avoir des triades ? Elles auraient sans aucun doute été beaucoup moins spécifiques, en quelque sorte « bonnes à tout faire ». Pourquoi pas ? La Figure 6 représente un tel exemple de triade très simplifiée. La stéréochimie de la molécule, ou « chiralité », y est précisée : c’est une question tout à fait essentielle, qu’un modèle complet d’origine de la vie se doit d’expliquer [4].

Enfin, nous n’imaginons pas la vie sans l’existence de structures cloisonnées, des cellules ou quelque chose qui y ressemble, donc des membranes ou des parois. Les premières membranes ont pu être formées de peptides enchevêtrés, ou plus ordonnés, collés les uns aux autres. Elles ont pu aussi contenir de longues chaines organiques hydrophobes, celles des acides gras (Figure 6). On sait justement synthétiser ces acides gras aujourd’hui grâce à des protéines et à la chimie des thiolesters.
Le monde où la vie est apparue qui se dessine alors serait un monde de peptides bien plus qu’un monde d’acides nucléiques. Le soufre, à travers la cystéine et les thiolesters, y aurait joué un rôle tout à fait central, ce qui le relie à un possible monde encore plus primitif, plus « minéral », le monde à fer-soufre [5],[6]. Cela amène à réfléchir au rôle spécifique qu’aurait pu jouer le fer ferreux, soluble, donc disponible, possible fournisseur d’électrons, donc d’énergie, en lien avec tous ces peptides.
Références et notes
Image de couverture. Montage EEnv à partir d’une image CC0 License [source https://www.pexels.com/photo/beach-dawn-dusk-ocean-189349/ ] et des structures chimiques dessinées par l’auteur
[1] https://fr.wikipedia.org/wiki/Lune. A propos de la naissance de la lune, on trouvera dans cet article des hypothèses alternatives à celle de l’impact géant.
[2] Goldford J.E., Hartman H., Smith T.F. & Segré D. (2017) Remnants of an ancient metabolism without phosphates. Cell 168, 1-9. http://dx.doi.org/10.1016/j.cell.2017.02.001
[3] https://fr.wikipedia.org/wiki/Hypothèse_du_monde_à_ARN
[4] https://fr.wikipedia.org/wiki/Chiralité_(chimie)
[5] https://fr.wikipedia.org/wiki/Protéine_fer-soufre
[6] Vallée Y., Shalayel I. et al. (2017) At the very beginning of life on Earth: The thiol-rich peptide (TRP) world hypothesis. Int. J. Dev. Biol. 61: 471-478. http://doi.org/10.1387/ijdb.170028yv
L’Encyclopédie de l’environnement est publiée par l’Association des Encyclopédies de l’Environnement et de l’Énergie (www.a3e.fr), contractuellement liée à l’université Grenoble Alpes et à Grenoble INP, et parrainée par l’Académie des sciences.
Pour citer cet article : VALLÉE Yannick (17 avril 2021), Il était une fois la vie : la chimie dans l’océan terrestre il y a 4 milliards d’années, Encyclopédie de l’Environnement. Consulté le 30 décembre 2024 [en ligne ISSN 2555-0950] url : https://www.encyclopedie-environnement.org/vivant/etait-vie-chimie-locean-terrestre-y-a-4-milliards-dannees/.
Les articles de l’Encyclopédie de l'environnement sont mis à disposition selon les termes de la licence Creative Commons BY-NC-SA qui autorise la reproduction sous réserve de : citer la source, ne pas en faire une utilisation commerciale, partager des conditions initiales à l’identique, reproduire à chaque réutilisation ou distribution la mention de cette licence Creative Commons BY-NC-SA.