环境中的硝酸盐

人们目前已经达成共识,农业是环境中硝酸盐的主要来源之一。这是由于大自然本身的氮循环作用以及农业化肥的使用。环境中存在低浓度的硝酸盐是一种难以避免的现象。然而,自然环境和我们消费的产品中的硝酸盐浓度很大程度上取决于农业实践。本文试图阐明农业土壤氮素管理中硝酸盐来源的问题。结果表明,氮肥管理需要制定新的策略,在制定策略的过程中也需要得到应有的帮助。
1. 农业集约化和硝酸盐渗漏到环境中
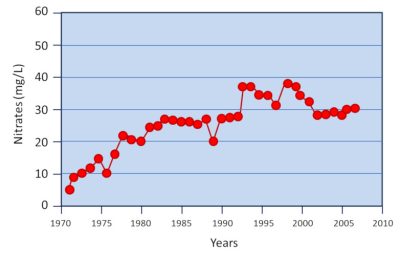
(图1 nitrates 硝酸盐;Years 年份)
在20世纪下半叶,西欧农业的特点是生产方式的集约化,特别是基于氮肥使用的发展。但随之而来的是内陆水域硝酸盐污染程度加剧,这一现象在现在已得到证实。自20世纪70年代以来,专业人士已经提出了一种策略,即根据植被的需求合理地调整氮肥施肥量以便更好地控制氮肥的使用。然而,地表水和地下水中硝酸盐浓度变化的数据表明,要控制环境中的这些泄漏仍有很长的路要走(图1)[1]。
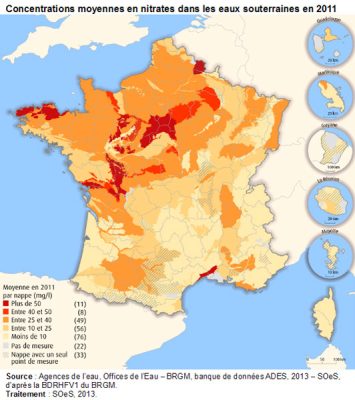
(图2 concentrations moyennes en nitrates dans les eaux souterraines en 2011 2011年地下水中硝酸盐的平均浓度;asinigue 阿西尼格;Gujdie:古迪;Magole:麦高乐;moyenne en 2011 2011年平均值;par nappe(mg/I) 每个区域(毫克/每升);Plus de 50(11) 大于50(11);Entre 40 et 50(8) 40到50之间(8);Entre 25et 40(49) 25到40之间(49);Entre 10et 25(56) 10到25之间(56)○11Moins de 10(76) 少于10(76);Pas de mesure(22) 没有测量;Nappe avec un seul(33) 只有一个区域;point de mesure 测量点;Source : Agences de l’eau, Offices de l’Eau – BRGM, banque de donnéesADES, 2013- SOeS, d’après la BDRHFV1 du BRGM. 资料来源:水务机构、水务办公室 – BRGM、ADES 数据库,2013-SOeS,根据 BRGM BDRHFV1;Traitement : SOeS, 2013. 处理:SOeS,2013 年。)
对其增长的观察可以扩大到整个法国,不同区域程度有所不同。法国西北部、罗纳河谷和阿尔萨斯平原的西南部这些农业集约化地区的污染程度最高(图2,[2])。这些观察结果引出了一系列的问题,我们将尝试提供一些答案。
2. 土壤和水中硝酸盐的形成机理
土壤和水中硝酸盐的形成是在环境自然作用下(图3)氮循环的一个阶段,氮循环是在土壤和水体中或多或少由特定微生物群作用导致的。
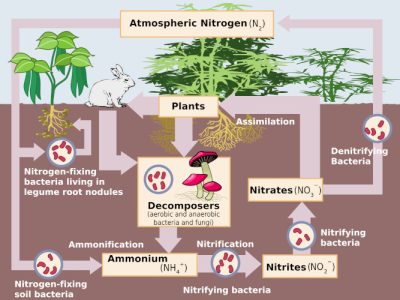
(图3 Azote atmospherique(N2) 气态氮;Oxyde nitieux(N2O) 一氧化二氮;Bactéries dénitrifiantes 反硝化细菌;Nitrates(NO3-):硝酸盐;Nitrites(NO2-) 亚硝酸盐;Bactéries nitrifiantes 硝化细菌;Nitrification 硝化;Ammonification:氨化;Ammoniaque(NH4+) 铵根;Bactéries fixatrices d’azote dans le sol 土壤固氮菌;Bactéries fixatrices d’azote nodules de légumineuses 豆类固氮根瘤菌)
在这些微生物群中,一些细菌群能够将大气中的惰性氮气(N2)转化为氨氮(NH4+)供植物使用,特别是与某些特定细菌相关的豆科植物(见共生和寄生)。植物吸收的氮可以用来合成植物蛋白质(R-NH2)和其他用于动物或人类营养的植物有机氮产品。随着动植物产品在土壤中的分解,这种有机氮再次转化为铵态氮(NH4+);有机质矿化是指土壤有机质(腐殖质)和近期掩埋的有机质的矿化。形成的铵态氮可以被植物再次使用,或通过硝化作用转化为亚硝酸盐(NO2–)然后进一步转化为硝酸盐(NO3–)。硝酸盐是土壤和水中氮的最高氧化形式,是高度可溶和可移动的矿物盐。这些硝酸盐可以被植物吸收,是许多栽培植物氮营养的基础。它们也可以被与植物存在竞争关系的土壤微生物所吸收。
在缺氧环境中,这些硝酸盐也可以被一些土壤细菌用来代替氧气进行呼吸作用:它们进行反硝化作用,将这些硝酸盐转化为亚硝酸盐,然后形成气态氮氧化物(NO和NO2),最后变成大气中惰性氮气(N2),从而回到氮循环的起点[3]。
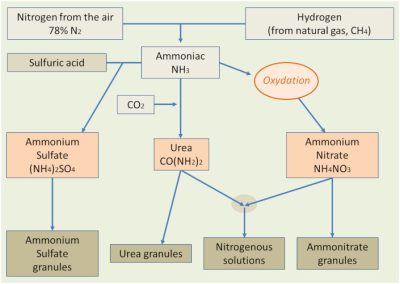
(图4 Azote de lair 78%N 空气中氮气(78%);Hydrogène(à partir de gaz naturel, CH4) 氢气(来自天然气,甲烷);Acide sulfurique 硫酸;Ammoniac NH3 氨(NH3);Oxydation 氧化;CO2 二氧化碳;Sulfate dammonium/ (NH4)2SO4 硫酸铵;Urée/CO(NH2)2 尿素;Nitrate dammonium/NH4NO3 硝酸铵;Sulfate Dammonium granulé 硫酸铵颗粒;Urée granulée 尿素颗粒;Solutions azotées 液氮;Ammonitrates granulé 硝酸铵颗粒)
因此,土壤中硝酸盐的存在是所有这些转化的结果。在自然环境中,土壤或水中的硝酸盐浓度通常较低,这表明形成的硝酸盐能够很快地被植物同化或微生物转化。因此,氮的可利用性往往是这些转化的一个限制因素。然而,无论是自然的还是人为的,在富含有机物的环境中硝酸盐的浓度可能会更高。因此,在智利鸟粪 的堆积是农业中使用的天然硝酸盐的来源,而在石灰岩墙上天然形成的硝石(硝酸钾)是住宅附近家庭氮排放的结果。
氮肥的工业生产(图4)主要是以氨、尿素或硝酸盐产品的形式,对农作物产量的增加产生了不可否认的影响,农作物产量的增加又反过来直接影响这些肥料的供应。然而,这些养分的输入也引起了自然环境中氮转化的增加,从而导致了上述泄漏的增加。
3. 水中硝酸盐含量的增加对健康有害吗?
这个问题在人类健康保护界中引起了许多争论。硝酸盐的高溶解度不仅促进了它们在土壤中的扩散,也促进了它们被植物吸收。然而,这也是它们在强降雨时期逃离根系区域、并迁移到地下水或河流的原因。因此,我们生活的环境是一个存在硝酸盐的自然环境。日常饮食中,,我们经常摄入硝酸盐,通常是低剂量的。它们来自蔬菜和水果,或通过或多或少富含有机物土壤过滤的水,甚至是由一些富含硝酸盐或亚硝酸盐(将两者作为食品防腐剂)的产品。在过去的一个世纪里,河流和地下水中硝酸盐浓度的升高引起了人们对其毒性的关注。因此,世界卫生组织(WHO)[4]通过综合研究,根据人的体重确定了饮食中硝酸盐的可接受日摄入量(ADI):3.7毫克硝酸根/每千克/每天(3.7 mg NO3–/kg/day),体重70公斤(kg)的人通常减少到250毫克/每天(250 mg/day )。
一些人认为摄入低剂量的硝酸盐对健康有益,因为它已被证明对血压和心脏功能有积极的影响[5]。然而,卫生当局的注意力主要集中在摄入的两种确定风险上:蓝婴病(也称高铁血红蛋白症),以及硝酸盐转化为亚硝酸盐过程中致癌物亚硝胺生成的可能性。众所周知,人体消化道中肠道微生物能够将硝酸盐转化为活性更强的亚硝酸盐,可以进入血液并附着于血红蛋白,大量亚硝酸盐会抑制血红蛋白运输氧气的功能。
因此,婴儿高铁血红蛋白症的原因在于摄入过多硝酸盐含量过高的水或食物导致形成亚硝酸盐。流行病学观察[6]促使世界卫生组织WHO基于这种病理的风险制定了饮用水中硝酸盐最大可接受浓度(50mg/L)的标准:尽管有争议,但世卫组织[5]重申了该标准的重要性,同时还强调了幼儿胃肠道感染风险的增加,这有利于硝酸盐还原为亚硝酸盐。
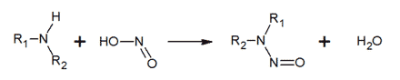
另一个潜在的危险源是这些亚硝酸盐可能形成致癌化合物。在实验室条件下,亚硝酸盐发生反应生成被广泛认为具有致癌特性的亚硝胺(图5)[7]。虽然一些亚硝胺可能在自然环境中形成,但它们在动物体内由摄入的硝酸盐形成亚硝胺仍然是科学家们讨论的一个话题[8]。根据对日益增加的癌症患者的流行病学研究,医学界重申了通过降低环境中亚硝基化合物前体,特别是硝酸盐[9]的浓度来限制接触亚硝基化合物的重要性[9]。
总之,通过饮食和饮用水摄入低剂量的硝酸盐几乎是不可避免的,且被认为对我们的健康没有不利影响。但摄入更高剂量的硝酸盐并非没有风险:这就是世卫组织建议一直监测供水管网中硝酸盐浓度的原因。
4. 水或土壤中的硝酸盐含量的增加对环境有害吗?
4.1. 硝酸盐与水生环境富营养化
地表水(河流和湖泊)和沿海水域可能会因为农业或城市地区矿物氮 (主要是硝酸盐)的排放而导致富营养化。这些泄漏是由于肥料或有机氮产品的过量使用,从而进入到河流或地表水库中。随后这些水域为水生植物和藻类生长提供了有利的环境,从而导致水体富营养化。
氮营养元素的输入通常伴随着含磷的生活废水排放到河流中,或伴随着动物排泄物(粪便、粪水)排放到农田中,促进水生植物生物量的激增。这些植物死亡时,其分解会消耗氧气,危害水生动物,并创造腐烂条件,产生恶臭的化合物,特别是硫化氢(H2S)。在法国,富营养化现象主要发生在阿尔卑斯山脉的湖泊中,但已经得到了控制(阿讷西湖),或者由于磷酸盐污染的减少而显著减少(日内瓦湖、布尔杰湖[10])。
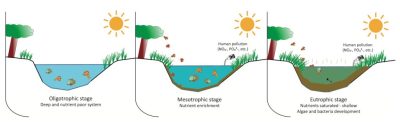
[来源:http://www.aquagreen-tech.com/en/presentation/eutrophisation.html]
(图6 Oligotrophe 贫养阶段;Mésotrophe:中养阶段;Eutrophe 富营养阶段;Pollition humaine 人类污染;Profond et pauvre en nutriment 重度营养贫瘠;Enrichissement en nutriments 营养丰富;Saturé en nutriments-peu profond 营养饱和-浅;Développement batérien et algal 微生物和藻类发育)
另一方面,这种藻类增殖及其腐烂的后果在布列塔尼沿海地区尤其显著,主要与过度施用牲畜粪便后硝酸盐的转移有关。通过分析磷酸盐和硝酸盐在这些藻类增殖中各自的作用,我们可以描述富营养化机制的演变(图6),并根据初始磷富集度描述介质的不同功能和植物生长所必需的低剂量元素。事实上,藻类和植物的生长既需要磷(或磷酸盐)来进行能量代谢,也需要氮(通常以硝酸盐的形式)来合成蛋白质。

因此,在山区湖泊中,最初的水中矿物质含量很低(所谓的寡养环境),富营养化现象是由生活污水排放的磷酸盐引起的。这些磷酸盐促进了蓝藻的生长,蓝藻是一种既有光合作用又有固定空气中氮以合成蛋白质功能的微生物。这些蓝藻也因其产生的蓝藻毒素而成为污染的来源。
另一方面,在沿海环境或地表水库中(图7),由于牲畜粪便使用过多和地表径流流经土壤,磷积累量很大,因此磷酸盐的可用性不是藻类生长的限制因素。观察到的限制其春季增殖的主要方法是减少氮(主要是以硝酸盐的形式)的可用性[1]。
4.2. 土壤硝酸盐和氮氧化物排放
在缺氧环境中,硝酸盐可用于反硝化细菌的呼吸过程,根据反应的顺序依次产生氧化程度较低的氮化合物:
硝酸盐(NO3–)→亚硝酸盐(NO2–)→一氧化氮(NO)→一氧化二氮(N2O)→气态氮(N2)
在这些转化过程中,一氧化氮(NO)和一氧化二氮或一氧化二氮(N2O)可能从发生这些转化的环境中排放出来,包括土壤。这两种气体都是空气污染物。一氧化氮是臭氧的前体,对低层大气中的植被有害。然而,与其他人为来源,特别是车辆排放的一氧化氮相比,来自土壤硝酸盐排放的一氧化氮的量很小。另一方面,一氧化二氮是一种强大的温室气体:它的浓度比二氧化碳的浓度低1000倍,但全球变暖潜势是二氧化碳的300倍,并且对温室效应的增强贡献了7.5%[11]。它在反硝化过程中的排放是这种气体主要的自然来源,其在大气中的浓度增加与氮肥的发展直接相关。限制这些气体的排放是目前农业氮管理面临的挑战之一,特别是在植物不需要硝酸盐的时候限制硝酸盐的可用性。
4.3. 硝酸盐和土壤有机质的破坏
硝酸盐是氮的最高氧化形式,它可以被植物吸收,然后进入有机化合物的形成过程。但如果没有被利用,这些硝酸盐最终会被反硝化。氮循环的总体平衡表明,以氮肥形式输入的复合氮在或多或少一段时期内会通过反硝化作用返回到大气中。然而,这个反应与有机质(CH2O)的氧化有关,如下所示:
4NO3– + 4H+ + 5CH2O→5CO2 + 2N2 + 7H2O
农学家们明白农业活动促进土壤有机质的矿化,特别是耕作有利于土壤通气性和微生物菌群氧化活性。然而,重要的是要记住,100公斤/公顷的氮气形式的氮构成了通过这种反硝化机制从土壤中氧化(从而消除)等量(107公斤/公顷)有机碳的能力。在管理土壤有机质方面,这一数量是不可忽略的,因为它对土壤的物理和生物功能也有有益的影响。这种破坏有机质的机制在分析土壤碳储量的变化和对其保存管理的思考中都没有考虑到。
5. 农业能减少它对环境造成的氮泄漏吗?
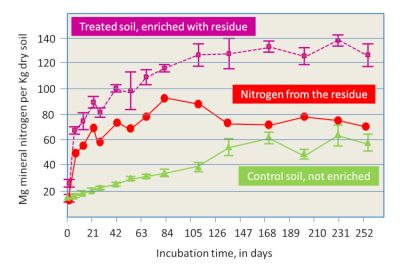
(图8 Sol traité, enrichi en résidu 处理过的富含残留物的土壤;Azote apporté par le résidu 残留物提供的氮;Sol témoin, non enrichi:不增肥的对照土壤;Durée d’incubation, en jours 孵化期,天;Mg d’azote mineral par Kg de sol sec 每公斤干燥土壤中矿物氮的镁含量)
在法国,地表水或地下水中硝酸盐污染来源于农业已被明确承认的,尽管这不是唯一的原因。生活或城市废水的排放可能是河流的污染源之一。然而,生物脱氮系统处理方法的发展往往能有效地限制这类污染。面对降低饮用水中硝酸盐浓度的需求,法国于2014年9月由于对农业氮污染管理松懈而被欧盟法院[12]谴责。这促使法国开始重审与农业界一起制定的氮肥剂量计算方法以符合欧洲水质法规。
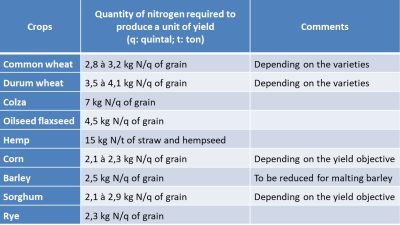
在作物生长之前,农民需要确定作物的氮输入量。他们的困难之一(难点之一)在于对氮的需求量的先验评估,以及确保在实践中氮的供应量与植被的需求相一致。重要的是要记住,栽培植物的生长在很大程度上取决于它们在生长过程中氮的可用性。表1这项试验使农学家确定了不同作物的需求比率(表1)。
农作物的氮输入一方面是基于估计的需求,另一方面是基于供应。这些在作物早期的估算可以根据作物的发展、环境条件的变化和环境知识进行调整。供应量应考虑到植物可获得的不同来源的氮供应:
- 土壤的供应是腐殖质形式的有机物矿化的结果,是由于土壤微生物群的活动而几乎连续不断释放矿物氮的结果。其产量主要取决于土壤中有机氮的储量及其生物降解性。它会随着土壤温度和湿度的变化而变化很大。我们知道如何定义这种有机库存的转化速率常数,从而评估这种供应。
- 土壤中有机残留物的供应,包括过去一年的作物残留物和可能的外部输入:如果残留物类型足够明确,矿物氮的供应可以通过残留物类型进行评估,或者通过实验工作评估(图8,[13])。这些有机残留物包括粪肥和其他牲畜产品,在使用氮肥之前,它们都是可用氮的来源。
在过去的50年里,耕种方式的简化导致了不同农场甚至不同地区作物和牲畜的分离。这导致了“田间作物”土壤中有机质输入的减少,因而难以维持其有机质储量。此外,将牲畜集中在专门的农场里,往往没有足够的土地来适当管理动物粪便中的氮。恢复作物和牲畜这两种耕作方式之间的功能联系似乎是良好土地管理的必要条件。但是,考虑到目前采用的操作方法,它似乎很难实施。
- 在农业历史上,豆类作物的氮供应可能是氮气中生物可利用氮进入农业系统的主要途径。这些作物可以从空气中获得氮合成植物蛋白质,而不经过硝酸盐阶段,并在土壤中留下有机残留物,作为后续农作物的矿质氮来源。
氮肥的易用性、农产品的销售价格和国际贸易协定是20世纪下半叶法国豆类作物急剧减少的原因。化肥成本的增加和生物固氮的环境效益(节省购买成本、限制温室气体排放、为后续作物提供土壤中的氮以及改善土壤维护等)目前正在推动这些作物的再发展。然而,这种发展在很大程度上取决于当地商业机会的潜力。
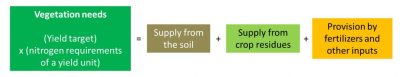
(图9 Besoins de la végétation 植被需求;objectif de rendement目标产量;(besoins azoté dune unité de rendement) 一个产量单位的氮需求;Fourniture par le sol 土壤的供应;Fourniture par les résidus de récolte 作物残留物的供应;Fourniture par les fertilisants et autres apports 肥料和其他投入的供应)
当其他来源的矿物质投入总量不能满足作物需求时,矿物肥料的供应当作为补充来源来补充作物的需求。氮肥料的易用性和灵活性,以及观察到的植物响应效果,是20世纪下半叶这些肥料蓬勃发展的原因。
然而,这种易用性也伴随着意想不到的副作用,即选择上可能突出了优先对施用的氮肥作出优先反应的作物品种。这表明豆科植物的选择是通过根据吸收土壤中的矿物质氮,而不是通过与微生物群结合来固定空气中的氮。我们还选择了在短时间内结籽的小麦品种,即在这种矿物氮供应的有效时间内结籽,而不是随时间推移更广泛地传播并提高土壤提供的氮的价值的氮营养品种……因此,植物选择受到当地农业实践的影响,从而增加了改变后者的难度。
在我们使用氮肥的种植系统中,氮元素管理是根据同样的概念模型来设计的:确定植物需求的数量和动态,并通过肥料提供除了土壤和作物残留物的供应外,还提供满足这些植物需求所需的氮量。法国使用的预测氮余额法(图9)也基于这种思路,其目的是限制泄漏,同时完全接受与环境波动或判断错误有关的偏差。
这种收支平衡法无疑使农民能够更好地使用氮肥,同时保持安全边际。考虑到氮供应的不同来源,我们能够在考虑到所有输入的情况下调整所需的用量。然而,这种来源的多样性也可能导致对每个项目的估计都有一定的安全边际,以及累积不确定性,从而导致对供应计算出的最终边际引起对预测评估价值的质疑[14]。这种希望保持足够操作空间的倾向在实践中很麻烦,不过可能解释了减少氮泄漏到水生环境中的困难!
然而,许多农民目前面临着生产成本的增加与收入的变化不同步的问题。一些农民意识到了与他们的活动有关的环境危害,以及采用不同最佳管理方法的可能性(经济、技术、生活质量),因此他们正在试图重新确定他们农场的经营方式,并对其投入 进行更严格的管理。有些农民倾向于有机农业的形式,并有着非常明确的规范。另一些人则试图通过重新发现更传统的农艺来提高他们的知识和技能。在氮管理方面,豆科作物的价值正在被重新发现,无论是作为主要作物还是作为辅助作物 ,或者是看中其在面临中等氮营养压力时不显著影响作物最终产量的情况下减少施肥的能力[15]。这些氮管理方法是在更广泛的范围内寻求更经济和环境友好的农业管理方法的一部分,还有一些工作致力于研究土壤管理方法和限制使用植物保护产品。在此背景下,人们关心的是保持足够的经济利润。
目前,旨在比较不同集约化水平下不同生产方式的科学和技术经济工作正在进行。这些不同的管理模式反映了农业实践方式真正在不断涌现,应该会出现新的结论和实践[16],[17]。对氮肥使用合理性的思考探寻也是这一不断演变的背景的一环。新策略正在形成,且需要得到应有的帮助。
参考资料及说明
封面照片:水生环境的富营养化,通常与过量的氮输入有关,这种氮主要来自农业的硝酸盐和废水[来源:F.Lamiot(CC by-SA 2.5),来自维基共享资源]。
[1] Chevassus-au-Louis B., Andral B., Feminas A. & Bouvier M. (2012) Bilan des connaissances scientifiques sur les causes de prolifération de macroalgues vertes – Application à la situation de la Bretagne et propositions. Ministry of Ecology and Sustainable Development and Ministry of Agriculture. 147 p. (in french)
[2] Ministère de l’Environnement, de l’Énergie et de la Mer (2013) Indicateurs de développement durable territoriaux. Les nitrates dans les eaux douces. 5p. Disponible à l’adresse :
http://www.statistiques.developpement-durable.gouv.fr/indicateurs-indices/f/1831/1328/nitrates-eaux-douces.html (Consulté en mars 2017) (in french)
[3] Albacore J.C. Philippot L. (2011) Denitrification. In: Handbook of Soil Sciences: Properties and Processes, pp. 32-40. Boca Raton, USA: CRC Press
[4] FAO/WHO (1996) Toxicological evaluation of certain food additives and contaminants. Geneva. World Health Organization, Joint FAO/WHO Expert Committee on food additives (WHO Food Additives Series N°35)
[5] WHO (2011) Nitrate and Nitrite in Drinking-water. Background document for development of WHO. Guidelines for drinking-water quality. 23p.
[6] Leclerc H. (2008) Nitrates de l’eau d’alimentation et risques pour la santé. Acad Agric Fr., 14 mai 2008, 4p. (in french)
[7] Hamon M. (2007) Les nitrates peuvent-ils induire une toxicité indirecte ? Ann. Pharm. Fr., 66, 347-355.
[8] Veena S. Rashmi S. (2014) A review on mechanism of nitrosamine formation, metabolism and toxicity in vivo. Int. J. Toxicol Pharm. Res., 6, 86-96.
[9] Conseil Supérieur d’Hygiène Publique de France (1996) Présentation et discussion d’un document élaboré par le Dr L’hirondel sur des normes et des recommandations concernant les nitrates. CR 13/02/1996. 5p. (in french)
[10] CIPEL (2015) Rapport Eaux du Léman – Campagne 2014, 261p ; Jacquet S. et al (2013) Suivi environnemental des eaux du lac du Bourget pour l’année 2012. Rapport INRA, CISALB, CALB, 226p. (in french)
[11] CITEPA (2015) Changement climatique et effet de serre : https://www.citepa.org. 11p (in french)
[12] Cour de Justice européenne (2014) Arrêt de la cour du 4 septembre 2014. Commission Européenne contre République française. Affaire C-237/12. (in french)
[13] Page S., Hénault C., Chèneby D., Lagacherie B. & Germon J.C. (1998) Devenir de l’azote des eaux résiduaires de féculerie Encyclopédie de l’environnement 11/11 Généré le 06/10/2021 après épandage sur un sol cultivé. Étude et Gestion des Sols, 5, 117-133. (in french)
[14] Germon J.C. (2013) Gestion de la fertilisation azotée en agriculture : enjeux environnementaux et perspectives agronomiques au niveau du territoire français. Cah Agric, 22, 241-248. (in french)
[15] Jeuffroy M.H., Gate P., Machet J.M. & Recous S. (2013) Gestion de l’azote en grandes cultures : les connaissances et outils disponibles permettent-ils de concilier exigences agronomiques et environnementales ? Cah. Agric., 22, 249-257. (in french)
[16] elarue J. & Cochet H. (2011) Proposition méthodologique pour l’évaluation des projets de développement agricole : l’évaluation systémique d’impact. Économie Rurale 323, pp. 36-54. (in french)
[17] Papy F. (2016) Les agricultures du monde face au dérèglement du climat. L’Encyclopédie du Développement Durable, 12p. (in french)
环境百科全书由环境和能源百科全书协会出版 (www.a3e.fr),该协会与格勒诺布尔阿尔卑斯大学和格勒诺布尔INP有合同关系,并由法国科学院赞助。
引用这篇文章: GERMON Jean-Claude (2025年1月4日), 环境中的硝酸盐, 环境百科全书,咨询于 2025年4月27日 [在线ISSN 2555-0950]网址: https://www.encyclopedie-environnement.org/zh/vivant-zh/nitrates-in-environment-2/.
环境百科全书中的文章是根据知识共享BY-NC-SA许可条款提供的,该许可授权复制的条件是:引用来源,不作商业使用,共享相同的初始条件,并且在每次重复使用或分发时复制知识共享BY-NC-SA许可声明。









